La plataforma de compras de realidad virtual inmersiva de Cleveland Clinic para la evaluación de actividades instrumentales de la vida diaria
Summary
La realidad virtual (VR) es un enfoque poderoso pero subutilizado para avanzar en el diagnóstico y tratamiento de enfermedades neurológicas. La plataforma de compras de realidad virtual de Cleveland Clinic combina contenido de realidad virtual de última generación con una cinta de correr omnidireccional para cuantificar las actividades instrumentales de la vida diaria, un marcador prodrómico propuesto de enfermedad neurológica.
Abstract
Se ha propuesto una disminución en el rendimiento de las actividades instrumentales de la vida diaria (IADL) como un marcador prodrómico de enfermedad neurológica. Las evaluaciones de IADL clínicas y basadas en el rendimiento existentes no son factibles para la integración en la medicina clínica. La realidad virtual (VR) es una herramienta poderosa pero subutilizada que podría avanzar en el diagnóstico y tratamiento de enfermedades neurológicas. Un impedimento para la adopción y el escalado de la RV en neurología clínica es la enfermedad relacionada con la RV que resulta de inconsistencias sensoriales entre los sistemas visual y vestibular (es decir, problema de locomoción).
La plataforma Cleveland Clinic Virtual Reality Shopping (CC-VRS) intenta resolver el problema de la locomoción combinando una cinta de correr omnidireccional con contenido de realidad virtual de alta resolución, lo que permite al usuario navegar físicamente por una tienda de comestibles virtual para simular compras. El CC-VRS consiste en experiencias de compra básicas y complejas; ambos requieren caminar 150 m y recuperar cinco elementos. La experiencia Complex tiene escenarios adicionales que aumentan las demandas cognitivas y motoras de la tarea para representar mejor el continuo de actividades asociadas con las compras en el mundo real. La plataforma CC-VRS proporciona resultados biomecánicos y cognitivos objetivos y cuantitativos relacionados con el rendimiento IADL del usuario. Los datos iniciales indican que el CC-VRS da como resultado una enfermedad VR mínima y es factible y tolerable para adultos mayores y pacientes con enfermedad de Parkinson (EP). Se revisan las consideraciones subyacentes al desarrollo, diseño y tecnología de hardware y software, y se proporcionan modelos iniciales de integración en atención primaria y neurología.
Introduction
En 2008, la Academia Nacional de Ingeniería identificó 14 Grandes Desafíos para la Ingeniería enel Siglo 211. Uno de ellos fue la integración de la realidad virtual (VR) en la medicina. Se ha avanzado en el uso de la RV para la formación de estudiantes de medicina 2,3, la planificación quirúrgica3, la reducción de la ansiedad asociada con las interacciones médicas4, la asistencia en el tratamiento del dolor agudo5 y el cáncer6, y el aumento de la recuperación motora después del accidente cerebrovascular7. A pesar de estas aplicaciones prometedoras, la utilidad de la RV en medicina no se ha realizado completamente, particularmente en el ámbito de la evaluación y el tratamiento de enfermedades neurológicas. Si bien los avances en la tecnología de realidad virtual han minimizado barreras como el costo, la comodidad de los auriculares y las características de usabilidad intuitivas, la enfermedad de realidad virtual continúa impidiendo la integración de la realidad virtual en la medicina8.
La enfermedad de realidad virtual se refiere a sentimientos similares al mareo por movimiento (por ejemplo, náuseas, vómitos, vértigo)9,10,11 que surgen durante las experiencias de realidad virtual. Aunque no hay una sola teoría acordada para explicar la enfermedad de la realidad virtual, la teoría del conflicto sensorial es una explicación principal12. Brevemente, la Teoría del Conflicto Sensorial sugiere que la enfermedad de la RV surge de las disparidades sensoriales; la información de flujo visual indica el movimiento hacia adelante del cuerpo a través del espacio, mientras que el sistema vestibular indica que el cuerpo está estacionario13. Esta discrepancia en la información sensorial resulta en un equilibrio deficiente, desorientación espacial y movimientos posturales incontrolables que son precursores de la enfermedad de la realidad virtual. Si bien se debate el mecanismo preciso que subyace a la enfermedad de RV, es probable que la reducción del desajuste entre las fuentes de información sensorial reduzca la enfermedad de VR14 y facilite la adopción de VR en un entorno médico.
La locomoción junto con la realidad virtual se ha propuesto durante mucho tiempo como un enfoque para reducir el desajuste sensorial al sumergir física y visualmente al usuario en el entorno virtual15,16. Varios estudios en adultos mayores con y sin enfermedad neurológica han emparejado con éxito los sistemas de realidad virtual inmersiva y no inmersiva con las cintas de correr unidireccionales tradicionales 17,18,19. Estos estudios demuestran que una intervención de RV y cinta de correr unidireccional suele ser bien tolerada18 y la intervención puede reducir la frecuencia decaídas 17,19. Estos resultados proporcionan una base prometedora para la integración exitosa de la locomoción y la realidad virtual. Sin embargo, el ritmo del motor externo de una cinta de correr unidireccional no permite al usuario cambiar de velocidad o ejecutar giros para interactuar con entornos virtuales realistas más complejos.
En las últimas dos décadas, los avances en hardware y software de seguimiento de movimiento han facilitado el desarrollo de entornos virtuales más inmersivos e interactivos. Un avance importante ha sido el desarrollo de la cinta de correr omnidireccional20. Brevemente, una cinta de correr omnidireccional utiliza simultáneamente movimientos lineales y rotacionales para permitir al usuario deambular en cualquier dirección a un ritmo autoseleccionado. Generalmente utilizadas en la industria del juego, las cintas de correr omnidireccionales amplían las oportunidades para aprovechar los entornos de realidad virtual en el entorno clínico al abordar el problema de la enfermedad de realidad virtual y facilitar la creación de entornos realistas que desafían mejor las capacidades físicas del usuario, como girar o cambiar de dirección. En particular, las réplicas virtuales de entornos cotidianos a gran escala pueden facilitar la evaluación del funcionamiento cognitivo y motor durante la realización de actividades instrumentales de la vida diaria (IADL).
Las actividades instrumentales de la vida diaria (IADL) son tareas funcionales (por ejemplo, ir de compras, tomar medicamentos, preparar alimentos) que son críticas para mantener una vida independiente21. La capacidad de lograr IADL comunes se ha propuesto como un marcador prodrómico para la enfermedad neurológica. Datos recientes de estudios prospectivos a largo plazo indican que las disminuciones en las IADL probablemente preceden a un diagnóstico de enfermedad de Parkinson (EP) a los 5-7 años 22,23 y un diagnóstico de enfermedad de Alzheimer 24,25. A diferencia de las actividades básicas de la vida diaria (BADL)26, las IADL suelen requerir la realización simultánea de dos tareas que demandan atención (por ejemplo, motor-cognitiva, motor-motora o cognitivo-cognitiva)27. La gran mayoría de las actividades diarias del hogar y la comunidad se realizan en condiciones de dobletarea 28,29.
Aunque las disminuciones de doble tarea afectan claramente el rendimiento de la IADL, las evaluaciones motoras clínicas tradicionales 30,31,32 y las pruebas neuropsicológicas 33,34 son insuficientes para evaluar las IADL, ya que estas evaluaciones separan la función en componentes discretos sin tener en cuenta su interdependencia. Los métodos actuales de evaluación directa de la IADL se basan en cuestionarios de autoinforme propensos a sesgos35 o evaluaciones largas y onerosas basadas en el desempeño36. Ninguno de los enfoques proporciona información objetiva y cuantitativa sobre el nivel de función de IADL de un individuo en el entorno comunitario.
Los avances en la tecnología de realidad virtual, junto con los avances de ingeniería subyacentes a las cintas de correr omnidireccionales, brindan la oportunidad de crear un entorno interactivo e inmersivo. Se crearon una tienda de comestibles virtual y una tarea de compras para evaluar simultáneamente el rendimiento motor, cognitivo, cognitivo-motor e IADL. La plataforma Cleveland Clinic Virtual Reality Shopping (CC-VRS) fue desarrollada en colaboración por un equipo de ingenieros biomédicos, desarrolladores de software, fisioterapeutas, terapeutas ocupacionales y neurólogos.
Se seleccionó una tarea de compra de comestibles para cuantificar el rendimiento de IADL en función de las recomendaciones de la Asociación Americana de Terapia Ocupacional26. La Virtual Multiple Errands Task (VMET)37, la Timed Instrumental ADL Scale38 y el Penn Parkinson’s Daily Activities Questionnaire-15 (PDAQ-15)39 reconocen las compras como un indicador importante del rendimiento motor y no motor asociado con la enfermedad neurológica. Otros han utilizado un auricular VR inmersivo para crear un entorno de tienda de comestibles en un intento de estimar el rendimiento de IADL 37,40,41. Sin embargo, no han evaluado un componente importante de las compras de comestibles: la locomoción. En general, los paradigmas actuales de la tienda de comestibles vr requieren que el participante use un controlador de mano para teletransportarse o navegar por un avatar por toda la tienda de comestibles. Nuestro objetivo era integrar la locomoción en la experiencia de compra virtual del usuario. El proceso de desarrollo de CC-VRS comenzó con un análisis formal de la tarea de una experiencia típica de una tienda de comestibles. Como se indica en la Figura 1, nueve componentes fundamentales de la tarea reflejan una combinación de elementos que pueden caracterizarse como actividades motoras, cognitivas o cognitivo-motoras necesarias para un rendimiento exitoso, como es característico de todos los IADL.
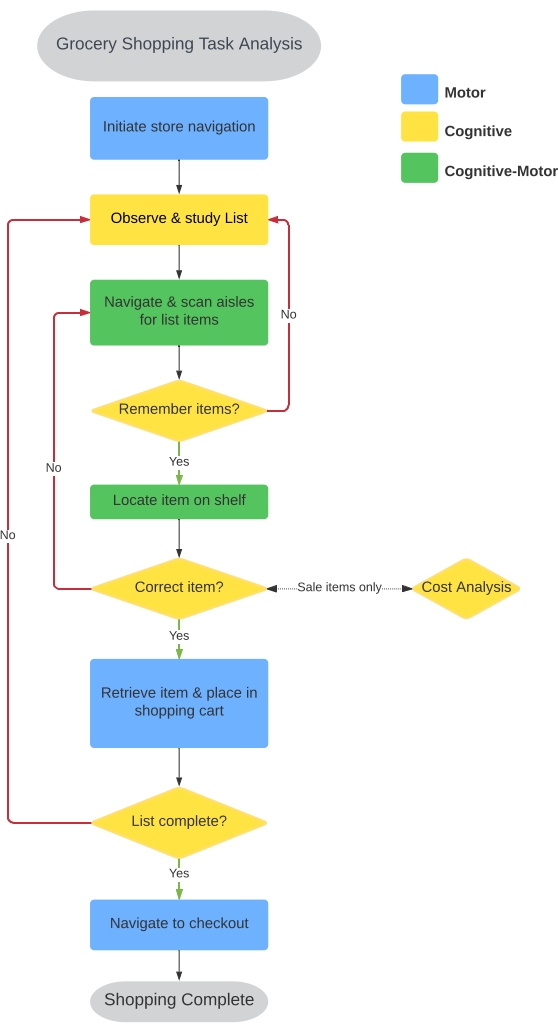
Figura 1: Análisis de tareas de compra de comestibles. Se realizó un análisis de tareas para identificar la secuencia de acciones y la naturaleza de esas acciones para la compra exitosa de comestibles en el mundo real. Se identificaron nueve secuencias primarias que se utilizaron para informar el desarrollo de las tareas de compra básicas y complejas . Las secuencias se clasificaron en motoras (azul), cognitivas (amarillas) y cognitivo-motoras (verdes); en la Tabla 1 se proporcionan detalles sobre los resultados correspondientes. Haga clic aquí para ver una versión más grande de esta figura.
La plataforma CC-VRS replica una tienda de comestibles realista y de tamaño mediano a través de un auricular VR inmersivo. Mientras camina en una cinta de correr omnidireccional, el usuario sigue una ruta continua y designada a través de la tienda, localiza artículos en una lista de compras y coloca los artículos en un carrito de compras virtual. Proporcionar una ruta designada estandariza la distancia recorrida a través de la tienda virtual, reduce el número de errores de navegación y facilita una mayor precisión para disociar los posibles cambios en el rendimiento de IADL de los errores de navegación o las estrategias de búsqueda subóptimas empleadas por el usuario. La ruta de 150 m requiere múltiples vueltas, lo que aumenta la complejidad motora42,43 y la probabilidad de desencadenar la congelación de la marcha en poblaciones de pacientes neurológicos, ya que las heladas se observan con mayor frecuencia durante el giro que la marcha en línea recta44,45. Tanto la distancia de la ruta de navegación como el número de elementos en la lista de compras pueden ser configurados por el médico para que coincidan con las habilidades del usuario o los objetivos de la sesión de evaluación.
Cada usuario completa un escenario de compras básico y otro complejo. El escenario básico simplemente requiere seguir la ruta y seleccionar artículos de la lista de compras. En el escenario complejo, al usuario se le proporciona una lista de diferentes artículos de comestibles mientras sigue la ruta idéntica a través de la tienda, pero se introducen demandas cognitivas y motoras adicionales (retiro verbal retrasado, comparación de precios y tareas de evitación de obstáculos descritas en la sección de protocolo a continuación). El ruido ambiental de la tienda de comestibles en los escenarios básico y complejo completa la experiencia inmersiva. Los datos resumidos y detallados sobre el rendimiento del usuario, incluidos los elementos correctos e incorrectos recopilados, el número y la frecuencia de las activaciones de la lista de compras, la duración de la parada y las métricas de la marcha, se generan automáticamente y están disponibles para su revisión por el médico.
El objetivo del CC-VRS es cuantificar objetivamente el rendimiento de las IADL en adultos mayores e individuos en riesgo o diagnosticados con enfermedad neurológica. El CC-VRS proporciona una experiencia inmersiva y realista para el usuario, y produce resultados precisos y biomecánicos de la función cognitiva y motora que tienen el potencial de servir como marcadores prodrómicos de enfermedades neurológicas o medidas objetivas de progresión de la enfermedad. El CC-VRS se está utilizando actualmente en tres proyectos relacionados destinados a: (1) comprender los efectos del envejecimiento saludable y las enfermedades neurológicas en el rendimiento de la IADL, (2) determinar la viabilidad de la integración clínica en la atención primaria y una clínica de trastornos del movimiento, y (3) identificar la firma neuronal subyacente a la congelación de la marcha en pacientes avanzados con EP con sistemas de estimulación cerebral profunda (DBS). Colectivamente, estos proyectos utilizarán la plataforma CC-VRS y los resultados asociados para comprender mejor cómo el envejecimiento y las enfermedades neurológicas afectan los aspectos del rendimiento de IADL. Este manuscrito detalla el desarrollo, el diseño y la tecnología de hardware y software del CC-VRS y sus nuevos resultados que pueden facilitar la integración en la atención médica.
Protocol
Representative Results
Discussion
La plataforma CC-VRS, hasta la fecha, parece abordar de manera más efectiva el problema de la locomoción en la realidad virtual al combinar contenido de realidad virtual de última generación con una cinta de correr omnidireccional. Un aspecto crítico del entorno inmersivo a la perfección del CC-VRS es garantizar una comunicación adecuada entre la cinta de correr y el software de realidad virtual. La configuración correcta de todos los aspectos del sistema de realidad virtual, incluidas las estaciones base, los rastreadores de pies y cintura, y los controladores manuales, es imperativa. Si el seguimiento es inconsistente o poco confiable, se requiere el ajuste de la orientación y la ubicación de las estaciones base, o la adición de otra unidad de estación base. La cobertura adecuada del espacio físico proporciona una sincronización estable entre el hardware de realidad virtual y la cinta de correr omnidireccional y garantiza que los datos de posición y orientación de los dispositivos de realidad virtual sean completos, precisos y precisos52. Se recomienda la calibración de la cinta de correr omnidireccional al comienzo de cada sesión de recopilación de datos para garantizar una responsividad óptima mientras se navega por el entorno virtual.
La familiarización del paciente con la cinta de correr es fundamental antes de administrar el CC-VRS. Aunque intuitiva y fácil de operar, la cinta de correr omnidireccional requiere la familiarización del usuario que se realiza mejor antes de la introducción de los auriculares VR y los desafíos de orientación espacial resultantes. Para satisfacer las necesidades del usuario individual y los objetivos de la presente evaluación, las siguientes características son configurables para cada escenario CC-VRS: 1) cinta de correr de baja o alta velocidad máxima, 2) repetición del módulo tutorial, 3) longitud de la ruta a través de la tienda y 4) número de artículos en la lista de compras. Estas modificaciones optimizan la evaluación de las capacidades cognitivas, motoras y de doble tarea de una amplia gama funcional de pacientes.
La falta de tecnología de plataforma única capaz de estandarizar el rendimiento de la IADL mediante el uso de resultados objetivos y cuantitativos que caracterizan el funcionamiento cognitivo y motor representa una barrera crítica en la identificación temprana y el tratamiento efectivo de enfermedades neurológicas relacionadas con la edad, como la EP o la enfermedad de Alzheimer. Los métodos actuales que estiman la función IADL utilizando cuestionarios de autoinforme, aunque son fáciles de administrar, son susceptibles de sesgo. Durante el autoinforme, los adultos mayores tienden a sobreestimar o subestimar las capacidades de IADL53. Del mismo modo, los informantes que completan las consultas de iaDL a menudo juzgan mal las capacidades debido a las percepciones erróneas de los observadores o las brechas de conocimiento35.
Una alternativa a los cuestionarios autoinformados y calificados por informantes es la evaluación IADL basada en el desempeño. Las evaluaciones basadas en el desempeño generalmente son completadas por un terapeuta ocupacional o físico capacitado. Si bien hay una serie de pruebas y guías de rendimiento disponibles, no son propicias para la integración en la atención clínica, ya que a menudo requieren mucho tiempo y espacio especializado y equipos que generalmente no se encuentran en el consultorio de un proveedor de atención primaria o neurología. Una de las evaluaciones basadas en el rendimiento más utilizadas, la Evaluación Directa del Estado Funcional (DAFS), requiere aproximadamente 40 minutos para administrarse, y su puntuación se basa en gran medida en la opinión experta del administrador de la prueba. Aunque el DAFS es útil en la estadificación de la enfermedad de Alzheimer, carece de sensibilidad y no detecta disminuciones de IADL en la etapa de deterioro cognitivo leve24. La fusión de los mundos virtual y real mediante la combinación de la realidad virtual con una cinta de correr omnidireccional brinda la oportunidad de capturar el rendimiento de IADL en condiciones cognitivas complejas que replican mejor los entornos del mundo real, lo que podría resultar en diagnósticos más tempranos de enfermedades neurológicas54.
La plataforma CC-VRS aborda la brecha clínica al proporcionar un enfoque estandarizado, sistemático, objetivo y cuantitativo para caracterizar las capacidades de IADL en adultos mayores y personas con enfermedades neurológicas. Sobre la base de pruebas y datos preliminares de usabilidad, los escenarios cc-VRS básicos y complejos se pueden completar en menos de 30 minutos. Al igual que otros estudios inmersivos de realidad virtual con EP18, la mayoría de las personas con EP experimentan síntomas leves de mareo por movimiento. Desde una perspectiva de usabilidad, el CC-VRS recibió una calificación general de SUS de 75.7, correspondiente a una letra de grado “B” y que se encuentra entre las categorías de descriptores “bueno” y “excelente”55. A modo de comparación, una evaluación reciente de aplicaciones populares de teléfonos y tabletas informa un puntaje promedio de SUS de 77.7 para las 10 aplicaciones principales en todas las plataformas56, incluidas las aplicaciones móviles como The Weather Channel y YouTube. Los comentarios de los participantes indicaron que la mayoría de los usuarios disfrutaron del realismo y la capacidad de interactuar con la plataforma CC-VRS. Es importante destacar que los participantes se sintieron desafiados desde un aspecto físico y cognitivo, lo que indica que el diseño logró su objetivo de crear una plataforma dinámica que recreara una experiencia IADL compleja.
Anteriormente hemos demostrado que la tecnología puede integrarse con éxito en los flujos de trabajo clínicos en la evaluación de pacientes con conmoción cerebral57 y en un servicio neurológico ocupado para pacientes con Esclerosis Múltiple (EM)58. Además, el uso de la tecnología en el manejo de la conmoción cerebral mejoró los resultados y redujo los costos59, mientras que su uso en el tratamiento de la EM condujo a un ahorro del 27% en el tiempo dedicado a documentar en la historia clínica electrónica para cada paciente60. Teniendo en cuenta el objetivo continuo de reducir el costo de la prestación de atención61 y que el tiempo dedicado a documentar en el registro electrónico de salud se cita con frecuencia para el agotamiento de losmédicos 62, es probable que la integración de la plataforma CC-VRS en la atención clínica proporcione un valor agregado sustancial a los sistemas hospitalarios. Dos proyectos están en curso en los que la plataforma CC-VRS se integra en 1) un centro regional de salud familiar de atención primaria que trata principalmente a adultos mayores sanos y 2) una clínica especializada en trastornos del movimiento en la Clínica Cleveland.
La ausencia de un biomarcador fisiológico o digital preciso y fiable para la EP y la enfermedad de Alzheimer causa grandes dificultades en el diagnóstico precoz y en la medición de la progresión de la enfermedad63,64. La plataforma CC-VRS tiene el potencial de proporcionar un biomarcador digital bajo una única plataforma tecnológica que mejorará la atención clínica y podría dar lugar a ensayos clínicos más cortos y eficientes al reducir la dependencia de los resultados clínicos subjetivos y altamente variables (por ejemplo, Movement Disorder Society – Unified Parkinson’s disease Rating Scale motor porción (MDS-UPDRS III)). La evaluación de la función motora y cognitiva en el campo de la neurología clínica no ha avanzado dramáticamente en las últimas tres décadas en términos de la evaluación de individuos con EP y los síntomas motores cardinales asociados, y mucho menos problemas cognitivos o de doble tarea. El avance más celebrado en la evaluación de individuos con EP es la revisión de la escala subjetiva de calificación clínica (MDS-UPDRS III). Es importante destacar que no creemos que el CC-VRS suplante al MDS-UPDRS III. Más bien, creemos que su mayor valor puede realizarse en las prácticas de atención primaria al proporcionar un enfoque estandarizado y objetivo para la cuantificación de las IADL. Si bien es prematuro creer que el CC-VRS en su forma actual es un marcador prodrómico de enfermedad neurológica, los resultados podrían usarse para levantar una bandera “roja” o “amarilla” en términos de funcionamiento neurológico que puede desencadenar una consulta por parte de un especialista en trastornos del movimiento, neuropsicología o geriatría. En cuanto a su uso en la atención clínica de la EP, se prevé que el CC-VRS podría utilizarse en la titulación de medicamentos o en la eventual programación de dispositivos de estimulación cerebral profunda. Tanto los casos de uso de Atención Primaria como los específicos de PD se encuentran actualmente en fase piloto. Al sumergir verdaderamente al usuario en un entorno realista y medir aspectos significativos e importantes de la función cognitiva y motora, el CC-VRS representa un paso inicial en la creación de un biomarcador digital potencialmente efectivo y escalable para enfermedades neurológicas.
El campo de la neurología clínica, en particular los trastornos del movimiento, está lleno de ejemplos de tecnología desarrollada para cuantificar un síntoma de EP único y aislado a través de acelerómetro u otras tecnologías de sensores 65,66,67,68,69. Hasta donde sabemos, ninguno de estos enfoques, aparte de nuestro balance 70,71,72,73 y las aplicaciones de temblor74, se han integrado en la atención clínica de rutina de la EP. La tecnología anterior a menudo es válida y confiable; sin embargo, la atención se ha centrado en el desarrollo de tecnología con poca consideración a la viabilidad de la integración clínica75,76. Los pacientes, proveedores, hospitales y organismos reguladores están cada vez más interesados en las medidas de resultado que cuantifican los cambios en las acciones diarias significativas 77,78,79,80. La integración clínica de medidas precisas y significativas de los síntomas neurológicos y el rendimiento de la IADL es necesaria para evaluar sistemáticamente la efectividad general de una intervención o determinar el potencial de una intervención para retrasar la progresión de la enfermedad. El desarrollo de un enfoque estandarizado para la evaluación de IADL adecuado para el uso clínico de rutina es atractivo para facilitar la comprensión integral y el tratamiento de la enfermedad neurológica en actividades significativas.
El enfoque CC-VRS para la evaluación del rendimiento de IADL para ayudar en el diagnóstico y manejo de enfermedades neurológicas tiene el potencial de transformar la atención médica a través del diagnóstico temprano y un seguimiento más preciso de la progresión de la enfermedad. Sin embargo, se reconoce plenamente que el sistema no está exento de limitaciones. El costo de la cinta de correr omnidireccional es sustancial y puede servir como una barrera para la adopción generalizada sin estudios sistemáticos de economía de la salud para identificar el posible punto de “equilibrio” entre el costo de la evaluación en relación con el valor del diagnóstico temprano o un seguimiento más preciso de la progresión de la enfermedad. En particular, las brechas en la adquisición de resultados centrados en el paciente de la EP con la tecnología fueron destacadas por el Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares PD Conference78, MDS Task Force on Technology77 y FDA. Pidieron tecnología que mida las actividades significativas de DP y la integración de estos resultados en la atención clínica. Actualmente estamos evaluando la integración del CC-VRS en un entorno de atención primaria y un centro de trastornos del movimiento en la Clínica Cleveland; estas implementaciones utilizarán cintas de correr omnidireccionales más asequibles. La recopilación exitosa de datos requiere una inversión inicial de tiempo por parte del médico para aprender a configurar y operar el sistema. Los pilotos clínicos en curso informarán mejor la cantidad de capacitación requerida para convertirse en un usuario competente. Uno podría imaginar un modelo en el que se emplea a un técnico para operar el sistema, y los pacientes completan las tareas de compra en lugar de sentarse en una sala de espera antes de una cita. Esos datos podrían integrarse instantáneamente en el registro de salud electrónico antes de ver a su proveedor. Este tipo de aplicaciones tienen el potencial de convertirse en la sala de espera del futuro para los pacientes.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Este estudio fue patrocinado por la Fundación Michael J. Fox para la Investigación del Parkinson (MJFF-020020) y la Cátedra de la Familia Edward y Barbara Bell. Agradecemos a Elm Park Labs (Detroit, MI) por su ayuda en la construcción del entorno de realidad virtual y la vinculación con la cinta de correr omnidireccional. También agradecemos a Evelyn Thoman y Brittney Moser por su ayuda con el desarrollo y la ejecución del proyecto.
Materials
| Cleanbox | Cleanbox | UV hygienic cleaning system used for disenfecting the VR headset | |
| Desktop PC | Dell | High-end gaming desktop | |
| Infinadeck Omnidirectional Treadmill | Infinadeck | Omnidirectional treadmill allows you walk in any direction | |
| Safety Harness | Ymachray | Standard saftey harness to prevent the patient from falling | |
| Valve Index Base Stations x3 | Valve | Tracking of the headset/controllers and trackers | |
| Valve Index Controllers (one set of 2) | Valve | Hand controllers to interact with the digital content | |
| Valve Index VR headset | Valve | VR headset | |
| Vive tracker 3.0 x3 | HTC | Placed on feet and waist to track position and control movement of treadmill | |
| Vive tracker straps | Skywin VR | Secures the Vive tracker around the waist | |
| Zip ties | Used to affix Vive trackers to shoelaces |
References
- Grand Challenges for Engineering. National Academy of Sciences Available from: https://16mhpx3atvadrnpip2kwi9or-wpengine.netdna-ssl.com/wp-content/uploads/2016/12/GrandChallenges.pdf (2008)
- Turso-Finnich, T., Jensen, R. O., Jensen, L. X., Konge, L., Thinggaard, E. Virtual reality head-mounted displays in medical education-a systematic review. Simulation in Healthcare. , (2022).
- Chen, T., et al. Virtual reality as a learning tool in spinal anatomy and surgical techniques. North American Spine Society Journal. 6, 100063 (2021).
- Gold, J. I., SooHoo, M., Laikin, A. M., Lane, A. S., Klein, M. J. Effect of an immersive virtual reality intervention on pain and anxiety associated with peripheral intravenous catheter placement in the pediatric setting: a randomized clinical trial. JAMA Network Open. 4 (8), 2122569 (2021).
- Huang, Q., Lin, J., Han, R., Peng, C., Huang, A. Using virtual reality exposure therapy in pain management: a systematic review and meta-analysis of randomized controlled trials. Value Health. 25 (2), 288-301 (2022).
- Groninger, H., Stewart, D., Wesley, D., Cowgill, J., Mete, M. Virtual reality for management of cancer pain: Study rationale and design. Contemporary Clinical Trials Communications. 26, 100895 (2022).
- Zhang, B., Li, D., Liu, Y., Wang, J., Xiao, Q. Virtual reality for limb motor function, balance, gait, cognition and daily function of stroke patients: A systematic review and meta-analysis. Journal of Advanced Nursing. 77 (8), 3255-3273 (2021).
- Saredakis, D., et al. Factors Associated with virtual reality sickness in head-mounted displays: a systematic review and meta-analysis. Frontiers in Human Neuroscience. 14, 96 (2020).
- Kim, H. K., Park, J., Choi, Y., Choe, M. Virtual reality sickness questionnaire (VRSQ): Motion sickness measurement index in a virtual reality environment. Applied Ergonomics. 69, 66-73 (2018).
- Cobb, S. V. G., Nichols, S., Ramsey, A., Wilson, J. R. Virtual reality-induced symptoms and effects (VRISE). Presence-Teleoperators and Virtual Environments. 8, 169-186 (1999).
- Kennedy, R., Lane, N., Lilienthal, M., Berbaum, K., Hettinger, L. Profile analysis of simulator sickness symptoms: application to virtual environment systems. Presence-Teleoperators and Virtual Environments. 1 (3), 295-301 (1992).
- Duzmanska, N., Strojny, P., Strojny, A. Can simulator sickness be avoided? a review on temporal aspects of simulator sickness. Frontiers in Psychology. 9, 2132 (2018).
- Reason, J. T. Motion sickness adaptation: a neural mismatch model. Journal of the Royal Society of Medicine. 71 (11), 819-829 (1978).
- Chance, S. S., Gaunet, F., Beall, A. C., Loomis, J. M. Locomotion mode affects the updating of objects encountered during travel: the contribution of vestibular and proprioceptive inputs to path integration. Presence Teleoperators & Virtual Environments. 7 (2), 168-178 (1998).
- Waller, D., Bachmann, E., Hodgson, E., Beall, A. C. The HIVE: a huge immersive virtual environment for research in spatial cognition. Behavior Research Methods. 39 (4), 835-843 (2007).
- Loomis, J. M., Blascovich, J. J., Beall, A. C. Immersive virtual environment technology as a basic research tool in psychology. Behavior Research Methods, Instruments, & Computers. 31 (4), 557-564 (1999).
- Mirelman, A., et al. Addition of a non-immersive virtual reality component to treadmill training to reduce fall risk in older adults (V-TIME): a randomised controlled trial. Lancet. 388 (10050), 1170-1182 (2016).
- Kim, A., Darakjian, N., Finley, J. M. Walking in fully immersive virtual environments: an evaluation of potential adverse effects in older adults and individuals with Parkinson’s disease. Journal of NeuroEngineering and Rehabilitation. 14 (1), 16 (2017).
- Pelosin, E., et al. Motor-cognitive treadmill training with virtual reality in Parkinson’s disease: the effect of training duration. Frontiers in Aging Neuroscience. 13, 753381 (2021).
- Darken, R. P., Cockayne, W. R., Carmein, D. The omni-directional treadmill: A locomotion device for virtual worlds. Proceedings of the 10th Annual ACM Symposium on User Interface Software and Technology. , 213-221 (1997).
- Guo, H. J., Sapra, A. . Instrumental Activity of Daily Living. , (2021).
- Darweesh, S. K., et al. Trajectories of prediagnostic functioning in Parkinson’s disease. Brain. 140 (2), 429-441 (2017).
- Foubert-Samier, A., et al. Cognitive and functional changes in prediagnostic phase of Parkinson disease: A population-based study. Parkinsonism & Related Disorders. 79, 40-46 (2020).
- Marshall, G. A., Amariglio, R. E., Sperling, R. A., Rentz, D. M. Activities of daily living: where do they fit in the diagnosis of Alzheimer’s disease. Neurodegenerative Disease Management. 2 (5), 483-491 (2012).
- Sikkes, S. A., et al. Assessment of instrumental activities of daily living in dementia: diagnostic value of the Amsterdam Instrumental Activities of Daily Living Questionnaire. Journal of Geriatric Psychiatry and Neurology. 26 (4), 244-250 (2013).
- American Occupational Therapy Association. Occupational therapy practice framework: domain and process. American Journal of Occupational Therapy. 56 (6), 609-639 (2002).
- MacPherson, S. E. Definition: Dual-tasking and multitasking. Cortex. 106, 313-314 (2018).
- O’Shea, S., Morris, M. E., Iansek, R. Dual task interference during gait in people with Parkinson disease: effects of motor versus cognitive secondary tasks. Physical Therapy. 82 (9), 888-897 (2002).
- Romero-Ayuso, D., et al. Assessment of cognitive instrumental activities of daily living: a systematic review. Disability and Rehabilitation. 43 (10), 1342-1358 (2019).
- Goetz, C. G., et al. Movement Disorder Society-sponsored revision of the Unified Parkinson’s Disease Rating Scale (MDS-UPDRS): scale presentation and clinimetric testing results. Movement Disorders. 23 (15), 2129-2170 (2008).
- Perlmutter, J. S. Assessment of Parkinson disease manifestations. Current Protocols in Neuroscience. , 1382-1387 (2009).
- Palmer, J. L., et al. Unified Parkinson’s Disease Rating Scale-Motor Exam: inter-rater reliability of advanced practice nurse and neurologist assessments). Journal of Advanced Nursing. 66 (6), 1382-1387 (2010).
- Neisser, U. On "Social Knowing". Personality and Social Psychology Bulletin. 6 (4), 601-604 (1980).
- Neisser, U. . Memory Observed: Remembering in Natural Contexts. , (1982).
- Jekel, K., et al. Mild cognitive impairment and deficits in instrumental activities of daily living: a systematic review. Alzheimer’s Research & Therapy. 7 (1), 17 (2015).
- Chisholm, D., Toto, P., Raina, K., Holm, M., Rogers, J. Evaluating capacity to live independently and safely in the community: Performance assessment of self-care skills. British Journal of Occupational Therapy. 77 (2), 59-63 (2014).
- Cipresso, P., et al. Virtual multiple errands test (VMET): a virtual reality-based tool to detect early executive functions deficit in Parkinson’s disease. Frontiers in Behavioral Neuroscience. 8, 405 (2014).
- Owsley, C., Sloane, M., McGwin, G., Ball, K. Timed instrumental activities of daily living tasks: relationship to cognitive function and everyday performance assessments in older adults. Gerontology. 48 (4), 254-265 (2002).
- Brennan, L., et al. The Penn Parkinson’s Daily Activities Questionnaire-15: Psychometric properties of a brief assessment of cognitive instrumental activities of daily living in Parkinson’s disease. Parkinsonism & Related Disorders. 25, 21-26 (2016).
- Arlati, S., et al. Acceptance and usability of immersive virtual reality in older adults with objective and subjective cognitive decline. Journal of Alzheimer’s Disease. 80 (3), 1025-1038 (2021).
- Porffy, L. A., et al. A novel virtual reality assessment of functional cognition: validation study. Journal of Medical Internet Research. 24 (1), 27641 (2022).
- Swanson, C. W., Fling, B. W. Discriminative mobility characteristics between neurotypical young, middle-aged, and older adults using wireless inertial sensors. Sensors. 21 (19), 6644 (2021).
- Yeh, T. T., Liang, P. J., Lee, S. C. Differences in walking-to-turning characteristics between older adult fallers and nonfallers: a prospective and observational study using wearable inertial sensors. International Journal of Rehabilitation Research. 45 (1), 53-57 (2022).
- Zach, H., et al. Identifying freezing of gait in Parkinson’s disease during freezing provoking tasks using waist-mounted accelerometry. Parkinsonism & Related Disorders. 21 (11), 1362-1366 (2015).
- Bhatt, H., Pieruccini-Faria, F., Almeida, Q. J. Dynamics of turning sharpness influences freezing of gait in Parkinson’s disease. Parkinsonism & Related Disorders. 19 (2), 181-185 (2013).
- Hoops, S., et al. Validity of the MoCA and MMSE in the detection of MCI and dementia in Parkinson disease. Neurology. 73 (21), 1738-1745 (2009).
- Bruck, S., Watters, P. A. Estimating cybersickness of simulated motion using the simulator sickness questionnaire (SSQ): A controlled study. Proceedings of the 2009 Sixth International Conference on Computer Graphics, Imaging and Visualization; Institute of Electrical and Electronics Engineers (IEEE). , 486-488 (2009).
- Kennedy, R. S., Lane, N. E., Berbaum, K. S., Lilienthal, M. G. Simulator sickness questionnaire: An enhanced method for quantifying simulator sickness. The International Journal of Aviation Psychology. 3 (3), 203-220 (1993).
- Brooke, S. . Usability Evaluation in Industry. , 189-194 (1996).
- Lewis, J. R., Sauro, J. The factor structure of the system usability scale. Human Centered Design. , 94-103 (2009).
- Sauro, J., Lewis, J. R. . Quantifying the User Experience: Practical Statistics for User Research. 2nd ed. , (2016).
- Niehorster, D. C., Li, L., Lappe, M. The accuracy and precision of position and orientation tracking in the HTC Vive virtual reality system for scientific research. i-Perception. 8 (3), 2041669517708205 (2017).
- Suchy, Y., Kraybill, M. L., Franchow, E. Instrumental activities of daily living among community-dwelling older adults: discrepancies between self-report and performance are mediated by cognitive reserve. Journal of Clinical and Experimental Neuropsychology. 33 (1), 92-100 (2011).
- Reppermund, S., et al. Impairment in instrumental activities of daily living with high cognitive demand is an early marker of mild cognitive impairment: the Sydney memory and ageing study. Psychological Medicine. 43 (11), 2437-2445 (2013).
- Bangor, A., Kortum, P. T., Miller, J. T. An empirical evaluation of the system usability scale. International Journal of Human-Computer Interaction. 24 (6), 574-594 (2008).
- Kortum, P., Sorber, M. Measuring the usability of mobile applications for phones and tablets. International Journal of Human-Computer Interaction. 31 (8), 518-529 (2015).
- Alberts, J. L., et al. Development and implementation of a multi-disciplinary technology enhanced care pathway for youth and adults with concussion. Journal of Visualized Experiments. (143), e58962 (2019).
- Rhodes, J. K., et al. Multiple Sclerosis performance test: technical development and usability. Advances in Therapy. 36 (7), 1741-1755 (2019).
- Alberts, J. L., et al. A technology-enabled concussion care pathway reduces costs and enhances care. Physical Therapy. 100 (1), 136-148 (2020).
- Macaron, G., et al. Technology-enabled assessments to enhance multiple sclerosis clinical care and research. Neurology Clinical Practice. 10 (3), 222-231 (2020).
- Porter, M. E. What is value in health care. The New England Journal of Medicine. 363 (26), 2477-2481 (2010).
- Sutton, J. M., Ash, S. R., Al Makki, A., Kalakeche, R. A. A daily hospital progress note that increases physician usability of the electronic health record by facilitating a problem-oriented approach to the patient and reducing physician clerical burden. The Permanente Journal. 23, (2019).
- Maetzler, W., et al. Modernizing daily function assessment in Parkinson’s disease using capacity, perception, and performance measures. Movement Disorders. 36 (1), 76-82 (2021).
- Stephenson, D., Badawy, R., Mathur, S., Tome, M., Rochester, L. Digital progression biomarkers as novel endpoints in clinical trials: a multistakeholder perspective. Journal of Parkinson’s Disease. 11, 103-109 (2021).
- Lu, M., et al. Vision-based estimation of MDS-UPDRS Gait scores for assessing Parkinson’s Disease motor severity. Medical Image Computing and Computer-Assisted Intervention. 12263, 637-647 (2020).
- Hobert, M. A., et al. Progressive gait deficits in Parkinson’s disease: a wearable-based biannual 5-year prospective study. Frontiers in Aging Neuroscience. 11, 22 (2019).
- Thorp, J. E., Adamczyk, P. G., Ploeg, H. L., Pickett, K. A. Monitoring motor symptoms during activities of daily living in individuals with Parkinson’s disease. Frontiers in Neurology. 9, 1036 (2018).
- Shawen, N., et al. Role of data measurement characteristics in the accurate detection of Parkinson’s disease symptoms using wearable sensors. Journal of NeuroEngineering and Rehabilitation. 17 (1), 52 (2020).
- Lu, R., et al. Evaluation of wearable sensor devices in Parkinson’s disease: a review of current status and future prospects. Parkinsons Disease. 2020, 4693019 (2020).
- Ozinga, S. J., Alberts, J. L. Quantification of postural stability in older adults using mobile technology. Experimental Brain Research. 232 (12), 3861-3872 (2014).
- Ozinga, S. J., et al. Three-dimensional evaluation of postural stability in Parkinson’s disease with mobile technology. NeuroRehabilitation. 41 (1), 211-218 (2017).
- Ozinga, S. J., Linder, S. M., Alberts, J. L. Use of mobile device accelerometry to enhance evaluation of postural instability in Parkinson disease. Archives of Physical Medicine and Rehabilitation. 98 (4), 649-658 (2017).
- Ozinga, S. J., Machado, A. G., Miller Koop, M., Rosenfeldt, A. B., Alberts, J. L. Objective assessment of postural stability in Parkinson’s disease using mobile technology. Movement Disorders. 30 (9), 1214-1221 (2015).
- Maldonado-Naranjo, A., Koop, M. M., Hogue, O., Alberts, J., Machado, A. Kinematic metrics from a wireless stylus quantify tremor and bradykinesia in Parkinson’s disease. Parkinson’s Disease. 2019, 6850478 (2019).
- Lingaiah, A., et al. Improving anxiety in Parkinson’s disease: A cautionary tale about mobile health technologies. Parkinsonism & Related Disorders. 73, 50-51 (2020).
- di Biase, L., et al. Quantitative analysis of bradykinesia and rigidity in Parkinson’s disease. Frontiers in Neurology. 9, 121 (2018).
- Espay, A. J., et al. Technology in Parkinson’s disease: Challenges and opportunities. Movement Disorders. 31 (9), 1272-1282 (2016).
- Sieber, B. A., et al. Prioritized research recommendations from the National Institute of Neurological Disorders and Stroke Parkinson’s Disease 2014 conference. Annals of Neurology. 76 (4), 469-472 (2014).
- van Uem, J. M., et al. Health-related quality of life in patients with Parkinson’s disease–A systematic review based on the ICF model. Neuroscience & Biobehavioral Reviews. 61, 26-34 (2016).
- Papadopoulos, E., Buracchio, T. Drug Development Tool (DDT) COA #000142. U.S. Food & Drug Administration. , (2021).

