没入型クリーブランドクリニックバーチャルリアリティショッピングプラットフォームは、日常生活の機器活動の評価のための
Summary
バーチャルリアリティ(VR)は、神経疾患の診断と治療を進めるための強力でありながら十分に活用されていないアプローチです。クリーブランドクリニックバーチャルリアリティショッピングプラットフォームは、最先端のVRコンテンツと無指向性トレッドミルを組み合わせて、神経疾患の前駆マーカーとして提案されている日常生活の機器活動を定量化します。
Abstract
日常生活の器械的活動(IADL)のパフォーマンスの低下は、神経学的疾患の前駆マーカーとして提案されている。既存の臨床的およびパフォーマンスベースのIADL評価は、臨床医学への統合には現実的ではありません。バーチャルリアリティ(VR)は、神経疾患の診断と治療を前進させることができる強力でありながら十分に活用されていないツールです。臨床神経学におけるVRの採用とスケーリングの障害は、視覚系と前庭系の間の感覚的不一致(すなわち、移動運動の問題)に起因するVR関連の病気である。
クリーブランドクリニックバーチャルリアリティショッピング(CC-VRS)プラットフォームは、全方向トレッドミルと高解像度VRコンテンツを結合することによって移動運動の問題を解決しようと試み、ユーザーが仮想食料品店を物理的にナビゲートしてショッピングをシミュレートできるようにします。CC-VRSは、基本的なショッピング体験と複雑なショッピング体験で構成されています。どちらも150 mを歩き、5つのアイテムを取得する必要があります。複雑なエクスペリエンスには、タスクの認知的および運動的要求を増やして、現実世界のショッピングに関連するアクティビティの連続性をよりよく表す追加のシナリオがあります。CC-VRSプラットフォームは、ユーザーのIADLパフォーマンスに関連する客観的かつ定量的な生体力学的および認知的結果を提供します。初期データは、CC-VRSがVR酔いを最小限に抑え、高齢者およびパーキンソン病(PD)患者にとって実現可能かつ忍容性であることを示している。開発、設計、ハードウェアおよびソフトウェア技術の根底にある考慮事項がレビューされ、プライマリケアおよび神経学への統合の初期モデルが提供されます。
Introduction
2008年、米国工学アカデミーは、21世紀の工学のための14のグランドチャレンジを特定しました1。その一つが、バーチャルリアリティ(VR)の医療への統合です。医学生2,3のトレーニング、手術計画3、医療相互作用に伴う不安の軽減4、急性5および癌関連疼痛の管理支援6、脳卒中7後の運動回復の増強のためのVRの使用において進歩が見られました。これらの有望なアプリケーションにもかかわらず、医学におけるVRの有用性は、特に神経疾患の評価と治療の領域において、完全には実現されていません。VR技術の進歩により、コスト、ヘッドセットの快適性、直感的なユーザビリティ機能などの障壁が最小限に抑えられましたが、VRの病気はVRの医学への統合を妨げ続けています8。
バーチャルリアリティの病気は、VR体験中に発生する乗り物酔い(吐き気、嘔吐、めまいなど)9,10,11に似た感情を指します。VR酔いを説明する際に単一の理論が合意されているわけではありませんが、感覚葛藤理論は主要な説明です12。簡単に言えば、感覚葛藤理論は、VR酔いは感覚格差から生じることを示唆しています。視覚的流れ情報は、身体が静止していることを示す一方、前庭系は、身体が静止していることを示す13。この感覚情報の不一致は、バランスの悪さ、空間的見当識障害、制御不能な姿勢運動をもたらし、VR酔いの前兆となります。VR酔いの根底にある正確なメカニズムは議論されているが、感覚情報のソース間のミスマッチを減らすことは、VR酔い14を減らし、医療現場でのVRの採用を促進する可能性が高い。
VRと結合された移動運動は、ユーザを仮想環境に物理的および視覚的に没頭させることによって感覚の不一致を低減するアプローチとして長い間提案されてきた15、16。神経疾患の有無にかかわらず高齢者を対象としたいくつかの研究では、没入型および非没入型VRシステムを従来の一方向トレッドミルと組み合わせることに成功しています17,18,19。これらの研究は、VRおよび単方向トレッドミル介入が典型的に忍容性が良好であり18、介入が落下頻度17,19を低下させる可能性があることを実証している。これらの結果は、移動とVRの統合を成功させるための有望な基盤を提供します。ただし、単方向トレッドミルの外部モーターペーシングでは、速度を変更したり、ターンを実行してより複雑な現実的な仮想環境と対話したりすることはできません。
過去20年間、動き追跡ハードウェアとソフトウェアの進歩により、より没入型でインタラクティブな仮想環境の開発が容易になりました。大きな進歩は、全方向性トレッドミル20の開発であった。簡単に言えば、無指向性トレッドミルは、線形運動と回転運動を同時に利用して、ユーザーが自己選択したペースで任意の方向に歩行できるようにします。ゲーム業界で一般的に利用されている無指向性トレッドミルは、VR酔いの問題に対処し、方向転換や方向転換など、ユーザーの身体能力によりよく挑戦する現実的な環境の作成を容易にすることで、臨床現場でVR環境を活用する機会を広げます。特に、実物大の日常環境の仮想複製は、日常生活の器械的活動(IADL)のパフォーマンス中の認知および運動機能の評価を容易にすることができる。
日常生活の道具的活動(IADL)は、自立生活を維持するために不可欠な機能的タスク(例えば、買い物、薬の服用、食品の準備)である21。一般的なIADLを達成する能力は、神経学的疾患の前駆マーカーとして提案されている。長期のプロスペクティブ研究からの最近のデータは、IADLの減少がパーキンソン病(PD)の診断に5〜7年22,23年、アルツハイマー病の診断に24,25年先行する可能性が高いことを示している。日常生活の基本的な活動(BADL)26とは対照的に、IADLは通常、注意を要求する2つのタスク(例えば、運動 – 認知、または認知 – 認知)の同時実行を必要とする27。毎日の家庭や地域社会の活動の大部分は、二重タスクの条件下で行われています28,29.
デュアルタスクの低下はIADLのパフォーマンスに明らかに影響するが、従来の臨床運動評価30、31、32および神経心理学的テスト33,34は、IADLを評価するには不十分であり、これらの評価は相互依存性を考慮せずに機能を離散的な構成要素に分離する。IADLの直接評価の現在の方法は、バイアスがかかりやすい自己報告アンケート35または長くて負担のかかるパフォーマンスベースの評価36に依存しています。どちらのアプローチも、コミュニティ環境におけるIADL機能の個々のレベルに関する客観的で定量的な洞察を提供しません。
VR技術の進歩は、全方向性トレッドミルの根底にあるエンジニアリングの進歩と相まって、インタラクティブで没入型の環境を作り出す機会を提供します。仮想食料品店とショッピングタスクは、モーター、認知、認知モーター、およびIADLのパフォーマンスを同時に評価するために作成されました。クリーブランドクリニックバーチャルリアリティショッピング(CC-VRS)プラットフォームは、生物医学エンジニア、ソフトウェア開発者、理学療法士、作業療法士、神経科医のチームによって共同開発されました。
米国作業療法協会26からの勧告に基づいてIADLのパフォーマンスを定量化するために、食料品の買い物タスクが選択された。仮想多重用事タスク(VMET)37、時限器械ADLスケール38、およびペン・パーキンソンの日常活動アンケート-15(PDAQ-15)39は、買い物を神経疾患に関連する運動および非運動能力の重要な指標として認識している。また、没入型VRヘッドセットを使用して食料品店の環境を作成し、IADLのパフォーマンス37,40,41を見積もる試みもあります。しかし、彼らは食料品の買い物の主要な構成要素である移動性を評価することに失敗しています。一般に、現在の VR 食料品店のパラダイムでは、参加者はハンドヘルド コントローラーを使用して、食料品店全体でアバターをテレポートまたはナビゲートする必要があります。私たちは、ユーザーの仮想ショッピング体験に移動を統合することを目指しています。CC-VRS開発プロセスは、典型的な食料品店の経験の正式なタスク分析から始まりました。図 1 に示すように、9 つの基本的なタスク コンポーネントは、すべての IADL の特徴と同様に、パフォーマンスを成功させるために必要なモーター、認知、または認知運動活動として特徴付けることができる要素のブレンドを反映しています。
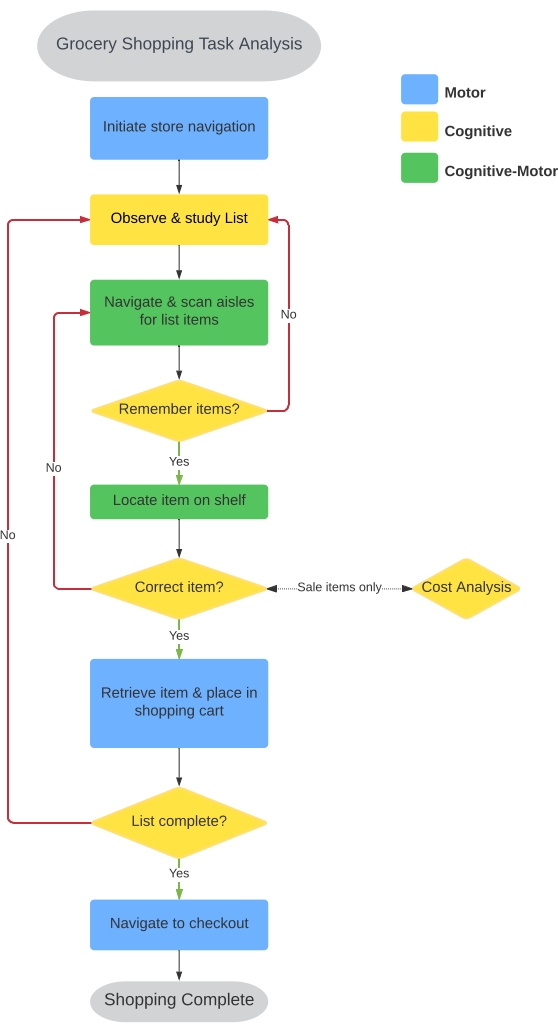
図1:食料品の買い物タスク分析 タスク分析を実行して、現実世界で食料品の買い物を成功させるための一連のアクションとそれらのアクションの性質を特定しました。9つの主要なシーケンスが同定され、 基本 および 複雑な ショッピングタスクの開発を知らせるために使用された。配列は、運動(青)、認知(黄色)、および認知運動(緑)に分類された。対応する結果に関する詳細は、 表1に示されている。 この図の拡大版を表示するには、ここをクリックしてください。
CC-VRSプラットフォームは、没入型VRヘッドセットを介してリアルで中規模の食料品店を再現します。全方向のトレッドミルを歩いている間、ユーザーは店舗を通る連続した指定されたルートをたどり、買い物リスト上のアイテムを見つけ、仮想ショッピングカートにアイテムを置きます。指定されたルートを提供することで、仮想ストア内を歩く距離が標準化され、ナビゲーションエラーの数が減少し、IADLパフォーマンスの潜在的な変化をナビゲーションエラーまたはユーザーが採用する最適でない検索戦略から切り離す際の精度が向上します。150mのルートは複数回のターンを必要とし、これは運動の複雑さを増大させ、神経学的患者集団における歩行の凍結を引き起こす確率は、直線歩行44,45よりも旋回中に凍結がより頻繁に観察されるためである44,45。ナビゲーション経路の距離および買い物リスト上のアイテムの数の両方を、臨床医が、ユーザーの能力または評価セッションの目標に一致させるように構成することができる。
各ユーザーは、1 つの基本ショッピング シナリオと 1 つの複合ショッピング シナリオを完了します。基本シナリオでは、ルートをたどり、買い物リストからアイテムを選択するだけです。複雑なシナリオでは、店舗を通る同一のルートをたどりながら、ユーザーにはさまざまな食料品のリストが提供されますが、追加の認知的および運動的要求が導入されます(以下のプロトコルセクションで説明する遅延口頭リコール、価格比較、および障害物回避タスク)。基本的なシナリオと複雑なシナリオの両方で周囲の食料品店の騒音は、没入型体験を完成させます。ユーザーのパフォーマンスに関する要約データと詳細データ (収集されたアイテムの正確と誤り、買い物リストのアクティブ化の数と頻度、停止期間、歩行メトリックなど) が自動的に生成され、臨床医によるレビューに利用できます。
CC-VRSの目標は、高齢者および神経疾患のリスクがある、または神経疾患と診断された個人におけるIADLのパフォーマンスを客観的に定量化することです。CC-VRSは、ユーザーに没入型でリアルな体験を提供し、神経学的疾患の前駆マーカーまたは疾患進行の客観的尺度として機能する可能性のある認知機能および運動機能の正確で生体力学的に基づく結果をもたらします。CC-VRSは現在、(1)IADLパフォーマンスに対する健康な老化と神経疾患の影響の理解、(2)プライマリケアおよび運動障害クリニックへの臨床統合の実現可能性の決定、および(3)深部脳刺激(DBS)システムを有する進行PD患者の歩行の凍結の根底にある神経シグネチャの同定を目的とした3つの関連プロジェクトで使用されています。これらのプロジェクトは、CC-VRSプラットフォームと関連するアウトカムを総合的に活用し、加齢と神経疾患がIADLのパフォーマンスの側面にどのように影響するかをよりよく理解します。この原稿では、CC-VRSの開発、設計、ハードウェアおよびソフトウェア技術と、医療への統合を容易にする新しい成果を詳述しています。
Protocol
Representative Results
Discussion
CC-VRSプラットフォームは、これまでのところ、最先端のVRコンテンツと全方向性のトレッドミルを組み合わせることで、VRの移動問題に最も効果的に対処しているようです。CC-VRSのシームレスな没入型環境の重要な側面は、トレッドミルとVRソフトウェア間の適切な通信を保証することです。基地局、足と腰のトラッカー、ハンドコントローラーなど、VRシステムのあらゆる側面を正しくセットアップすることが不可欠です。トラッキングに一貫性がない、または信頼性が低い場合は、基地局の向きや配置の調整、または別の基地局ユニットの追加が必要です。物理空間を適切にカバーすることで、VRハードウェアと全方向トレッドミル間の安定した同期が提供され、VRデバイスからの位置と向きのデータが完全、正確、正確であることが保証されます52。全方向トレッドミルのキャリブレーションは、仮想環境をナビゲートしながら最適な責任性を確保するために、すべてのデータ収集セッションの開始時に推奨されます。
CC-VRSを投与する前に、患者がトレッドミルに慣れていることが重要です。直感的で操作が簡単ですが、全方向トレッドミルには、VRヘッドセットの導入前に行うのに最適なユーザー慣れが必要であり、その結果生じる空間的向きの課題があります。個々のユーザーのニーズと現在の評価の目標を満たすために、CC-VRSシナリオごとに、1)トレッドミルの低速または最高速度、2)チュートリアルモジュールの繰り返し、3)店舗を通るルートの長さ、および4)買い物リストのアイテム数。これらの変更により、幅広い機能的患者の認知能力、運動能力、およびデュアルタスク能力の評価が最適化されます。
認知機能および運動機能を特徴付ける客観的および定量的結果を使用してIADL性能を標準化できる単一プラットフォーム技術の欠如は、PDまたはアルツハイマー病などの加齢性神経疾患の早期同定および効果的な治療における重要な障壁を表す。自己報告アンケートを用いてIADL機能を推定する現在の方法は、管理が容易であるが、バイアスの影響を受けやすい。自己申告中、高齢者はIADLの能力を過大評価または過小評価する傾向がある53。同様に、IADLクエリを完了した情報提供者は、オブザーバーの誤解や知識のギャップのために能力を判断することがよくあります35。
自己申告およびインフォーマント評価のアンケートに代わるものとして、パフォーマンスベースのIADL評価があります。パフォーマンスベースの評価は、通常、訓練を受けた作業療法士または理学療法士によって完了されます。多くのパフォーマンステストとガイドが利用可能ですが、それらは臨床ケアへの統合には役立たず、多くの場合、プライマリケアまたは神経学プロバイダーのオフィスでは一般的に見られない十分な時間と特殊なスペースと機器を必要とします。最も広く使用されているパフォーマンスベースの評価の1つである機能ステータスの直接評価(DAFS)は、管理に約40分を必要とし、そのスコアリングは主にテスト管理者の専門家の意見に基づいています。DAFSはアルツハイマー病の病期分類に有用であるが、感受性を欠き、軽度認知障害ステージ24におけるIADL低下を検出しない。VRと全方向性トレッドミルを組み合わせることで仮想世界と現実世界を融合させることで、現実世界の環境をよりよく再現する複雑な認知条件下でIADLのパフォーマンスをキャプチャする機会が得られ、神経疾患の早期診断につながる可能性があります54。
CC-VRSプラットフォームは、高齢者および神経疾患を有する人々のIADL能力を特徴付けるための標準化された体系的、客観的、定量的アプローチを提供することにより、臨床的ギャップに対処する。予備的なユーザビリティテストとデータに基づいて、基本シナリオと複雑なCC-VRSシナリオは30分以内に完全に完了できます。PD18を用いた他の没入型VR研究と同様に、PD患者の大多数は軽度の乗り物酔いの症状を経験しています。ユーザビリティの観点から、CC-VRSは75.7の全体的なSUS評価を受け、文字グレード「B」に対応し、「良い」と「優れた」記述子カテゴリ55の間に落ちた。比較のために、人気のある携帯電話やタブレットのアプリケーションを最近評価すると、The Weather ChannelやYouTubeなどのモバイルアプリケーションを含む、すべてのプラットフォーム56の上位10のアプリケーションの平均SUSスコアが77.7と報告されています。参加者からのコメントによると、ほとんどのユーザーはCC-VRSプラットフォームと対話するリアリズムと能力を楽しんでいました。重要なことに、参加者は身体的および認知的側面から挑戦を感じ、複雑なIADL体験を再現するダイナミックなプラットフォームを作成するという目標をデザインが達成したことを示しています。
我々は以前、脳震盪患者の評価57 および多発性硬化症(MS)患者のための忙しい神経学的サービスにおいて、技術が臨床ワークフローに首尾よく統合できることを実証した58。さらに、脳震盪の管理における技術の使用は、転帰を改善し、コストを削減し59、MSの治療におけるその使用は、各患者60の電子健康記録に文書化するのに費やす時間を27%節約した。ケア61 を提供するコストを削減するという継続的な目標と、医師のバーンアウト62のために電子カルテに文書化するのに費やされた時間が頻繁に引用されていることを考えると、CC-VRSプラットフォームの臨床ケアへの統合は、病院システムに実質的な付加価値を提供する可能性があります。CC-VRSプラットフォームを、1)主に健康な高齢者を治療する地域のプライマリケア家族保健センターと、2)クリーブランドクリニックの運動障害専門クリニックに統合する2つのプロジェクトが進行中です。
PDおよびアルツハイマー病の正確で信頼性の高い生理学的またはデジタルバイオマーカーの欠如は、早期診断および疾患進行の測定において大きな困難を引き起こす63,64。CC-VRSプラットフォームは、単一の技術プラットフォームの下でデジタルバイオマーカーを提供する可能性を秘めており、主観的で変動の激しい臨床転帰への依存を減らすことによって、臨床ケアを強化し、より短く効率的な臨床試験をもたらす可能性があります(例えば、運動障害学会 – 統一パーキンソン病評価尺度運動部分(MDS-UPDRS III))。臨床神経学の分野における運動機能および認知機能の評価は、認知的または二重課題の問題は言うまでもなく、PDおよび関連する基本的な運動症状を有する個人の評価に関して、過去30年間劇的に進歩していない。PDを有する個人の評価における最も有名な進歩は、主観的臨床評価尺度(MDS-UPDRS III)の改訂である。重要なのは、CC-VRSがMDS-UPDRS IIIに取って代わるとは考えていないことです。むしろ、IADLの定量化に標準化された客観的なアプローチを提供することによって、プライマリケアの実践においてその最大の価値が実現される可能性があると考えています。現在の形態のCC-VRSが神経疾患の前駆マーカーであると考えるのは時期尚早ですが、その結果は、運動障害、神経心理学、または老年医学の専門家による相談を引き起こす可能性のある神経学的機能に関して「赤」または「黄色」のフラグを上げるために使用できます。PD臨床ケアにおけるCC-VRSの使用に関しては、投薬の滴定や脳深部刺激装置の最終的なプログラミングに利用されることが期待されています。プライマリケアとPD固有のユースケースの両方が現在パイロット段階にあります。CC-VRSは、ユーザーを現実的な環境に真に没頭させ、認知機能および運動機能の有意義で重要な側面を測定することにより、神経疾患に対する潜在的に効果的でスケーラブルなデジタルバイオマーカーの作成における最初のステップを表します。
臨床神経学、特に運動障害の分野は、加速度計または他のセンサ技術を介して単一の単離されたPD症状を定量化するために開発された技術の例で満たされている65、66、67、68、69。我々の知る限り、これらのアプローチのいずれも、我々のバランス70、71、72、73および振戦アプリケーション74を除いて、日常的なPD臨床ケアに統合されていない。以前の技術は、多くの場合、有効で信頼性があります。しかし、焦点は臨床統合の実現可能性をほとんど考慮せずに技術開発にありました75,76。患者、医療提供者、病院、および規制機関は、有意義な日常行動の変化を定量化するアウトカム測定にますます関心を寄せています77,78,79,80。神経学的症状とIADLパフォーマンスの正確で有意義な測定値の臨床的統合は、介入の全体的な有効性を体系的に評価するか、疾患の進行を遅らせるための介入の可能性を決定するために必要である。日常的な臨床使用に適したIADL評価への標準化されたアプローチの開発は、有意義な活動に関する神経疾患の包括的な理解と治療を促進するために魅力的である。
神経疾患の診断と管理を支援するIADL性能の評価に対するCC-VRSアプローチは、早期診断と疾患進行のより正確な追跡を通じて医療を変革する可能性を秘めています。ただし、システムに制限がないわけではないことは完全に認識されています。全方向性トレッドミルのコストは相当なものであり、早期診断の価値に対する評価のコストまたは疾患進行のより正確な追跡との間の潜在的な「損益分岐点」を特定するための体系的な健康経済学研究以外の広範な採用の障壁として役立つ可能性がある。特に、PD患者中心のアウトカムを技術で獲得することのギャップは、国立神経障害・脳卒中研究所PD会議78、MDS技術タスクフォース77、およびFDAによって強調された。彼らは、有意義なPD活動を測定する技術と、これらの転帰を臨床ケアに統合することを求めた。私たちは現在、クリーブランドクリニックのプライマリケア環境と運動障害センターへのCC-VRSの統合を評価しています。これらの展開では、より手頃な価格の全方向性トレッドミルが利用されます。データの収集を成功させるには、臨床医がシステムのセットアップ方法と操作方法を学ぶために初期投資の時間が必要です。進行中の臨床パイロットは、熟練したユーザーになるために必要なトレーニングの量をよりよく知らせます。技術者がシステムを操作し、患者が予約前に待合室に座るのではなく、ショッピングタスクを完了するモデルを想像することができます。これらのデータは、プロバイダーに会う前に電子健康記録に瞬時に統合できます。これらのタイプのアプリケーションは、患者にとって将来の待合室になる可能性を秘めています。
Disclosures
The authors have nothing to disclose.
Acknowledgements
この研究は、Michael J. Fox Foundation for Parkinson’s Research (MJFF-020020)とEdward and Barbara Bell Family Chairが後援した。Elm Park Labs(ミシガン州デトロイト)には、VR環境の構築と全方向性トレッドミルとのリンクに協力してくれたことに感謝します。また、イヴリン・トーマンとブリトニー・モーザーのプロジェクト開発と実行への支援にも感謝します。
Materials
| Cleanbox | Cleanbox | UV hygienic cleaning system used for disenfecting the VR headset | |
| Desktop PC | Dell | High-end gaming desktop | |
| Infinadeck Omnidirectional Treadmill | Infinadeck | Omnidirectional treadmill allows you walk in any direction | |
| Safety Harness | Ymachray | Standard saftey harness to prevent the patient from falling | |
| Valve Index Base Stations x3 | Valve | Tracking of the headset/controllers and trackers | |
| Valve Index Controllers (one set of 2) | Valve | Hand controllers to interact with the digital content | |
| Valve Index VR headset | Valve | VR headset | |
| Vive tracker 3.0 x3 | HTC | Placed on feet and waist to track position and control movement of treadmill | |
| Vive tracker straps | Skywin VR | Secures the Vive tracker around the waist | |
| Zip ties | Used to affix Vive trackers to shoelaces |
References
- Grand Challenges for Engineering. National Academy of Sciences Available from: https://16mhpx3atvadrnpip2kwi9or-wpengine.netdna-ssl.com/wp-content/uploads/2016/12/GrandChallenges.pdf (2008)
- Turso-Finnich, T., Jensen, R. O., Jensen, L. X., Konge, L., Thinggaard, E. Virtual reality head-mounted displays in medical education-a systematic review. Simulation in Healthcare. , (2022).
- Chen, T., et al. Virtual reality as a learning tool in spinal anatomy and surgical techniques. North American Spine Society Journal. 6, 100063 (2021).
- Gold, J. I., SooHoo, M., Laikin, A. M., Lane, A. S., Klein, M. J. Effect of an immersive virtual reality intervention on pain and anxiety associated with peripheral intravenous catheter placement in the pediatric setting: a randomized clinical trial. JAMA Network Open. 4 (8), 2122569 (2021).
- Huang, Q., Lin, J., Han, R., Peng, C., Huang, A. Using virtual reality exposure therapy in pain management: a systematic review and meta-analysis of randomized controlled trials. Value Health. 25 (2), 288-301 (2022).
- Groninger, H., Stewart, D., Wesley, D., Cowgill, J., Mete, M. Virtual reality for management of cancer pain: Study rationale and design. Contemporary Clinical Trials Communications. 26, 100895 (2022).
- Zhang, B., Li, D., Liu, Y., Wang, J., Xiao, Q. Virtual reality for limb motor function, balance, gait, cognition and daily function of stroke patients: A systematic review and meta-analysis. Journal of Advanced Nursing. 77 (8), 3255-3273 (2021).
- Saredakis, D., et al. Factors Associated with virtual reality sickness in head-mounted displays: a systematic review and meta-analysis. Frontiers in Human Neuroscience. 14, 96 (2020).
- Kim, H. K., Park, J., Choi, Y., Choe, M. Virtual reality sickness questionnaire (VRSQ): Motion sickness measurement index in a virtual reality environment. Applied Ergonomics. 69, 66-73 (2018).
- Cobb, S. V. G., Nichols, S., Ramsey, A., Wilson, J. R. Virtual reality-induced symptoms and effects (VRISE). Presence-Teleoperators and Virtual Environments. 8, 169-186 (1999).
- Kennedy, R., Lane, N., Lilienthal, M., Berbaum, K., Hettinger, L. Profile analysis of simulator sickness symptoms: application to virtual environment systems. Presence-Teleoperators and Virtual Environments. 1 (3), 295-301 (1992).
- Duzmanska, N., Strojny, P., Strojny, A. Can simulator sickness be avoided? a review on temporal aspects of simulator sickness. Frontiers in Psychology. 9, 2132 (2018).
- Reason, J. T. Motion sickness adaptation: a neural mismatch model. Journal of the Royal Society of Medicine. 71 (11), 819-829 (1978).
- Chance, S. S., Gaunet, F., Beall, A. C., Loomis, J. M. Locomotion mode affects the updating of objects encountered during travel: the contribution of vestibular and proprioceptive inputs to path integration. Presence Teleoperators & Virtual Environments. 7 (2), 168-178 (1998).
- Waller, D., Bachmann, E., Hodgson, E., Beall, A. C. The HIVE: a huge immersive virtual environment for research in spatial cognition. Behavior Research Methods. 39 (4), 835-843 (2007).
- Loomis, J. M., Blascovich, J. J., Beall, A. C. Immersive virtual environment technology as a basic research tool in psychology. Behavior Research Methods, Instruments, & Computers. 31 (4), 557-564 (1999).
- Mirelman, A., et al. Addition of a non-immersive virtual reality component to treadmill training to reduce fall risk in older adults (V-TIME): a randomised controlled trial. Lancet. 388 (10050), 1170-1182 (2016).
- Kim, A., Darakjian, N., Finley, J. M. Walking in fully immersive virtual environments: an evaluation of potential adverse effects in older adults and individuals with Parkinson’s disease. Journal of NeuroEngineering and Rehabilitation. 14 (1), 16 (2017).
- Pelosin, E., et al. Motor-cognitive treadmill training with virtual reality in Parkinson’s disease: the effect of training duration. Frontiers in Aging Neuroscience. 13, 753381 (2021).
- Darken, R. P., Cockayne, W. R., Carmein, D. The omni-directional treadmill: A locomotion device for virtual worlds. Proceedings of the 10th Annual ACM Symposium on User Interface Software and Technology. , 213-221 (1997).
- Guo, H. J., Sapra, A. . Instrumental Activity of Daily Living. , (2021).
- Darweesh, S. K., et al. Trajectories of prediagnostic functioning in Parkinson’s disease. Brain. 140 (2), 429-441 (2017).
- Foubert-Samier, A., et al. Cognitive and functional changes in prediagnostic phase of Parkinson disease: A population-based study. Parkinsonism & Related Disorders. 79, 40-46 (2020).
- Marshall, G. A., Amariglio, R. E., Sperling, R. A., Rentz, D. M. Activities of daily living: where do they fit in the diagnosis of Alzheimer’s disease. Neurodegenerative Disease Management. 2 (5), 483-491 (2012).
- Sikkes, S. A., et al. Assessment of instrumental activities of daily living in dementia: diagnostic value of the Amsterdam Instrumental Activities of Daily Living Questionnaire. Journal of Geriatric Psychiatry and Neurology. 26 (4), 244-250 (2013).
- American Occupational Therapy Association. Occupational therapy practice framework: domain and process. American Journal of Occupational Therapy. 56 (6), 609-639 (2002).
- MacPherson, S. E. Definition: Dual-tasking and multitasking. Cortex. 106, 313-314 (2018).
- O’Shea, S., Morris, M. E., Iansek, R. Dual task interference during gait in people with Parkinson disease: effects of motor versus cognitive secondary tasks. Physical Therapy. 82 (9), 888-897 (2002).
- Romero-Ayuso, D., et al. Assessment of cognitive instrumental activities of daily living: a systematic review. Disability and Rehabilitation. 43 (10), 1342-1358 (2019).
- Goetz, C. G., et al. Movement Disorder Society-sponsored revision of the Unified Parkinson’s Disease Rating Scale (MDS-UPDRS): scale presentation and clinimetric testing results. Movement Disorders. 23 (15), 2129-2170 (2008).
- Perlmutter, J. S. Assessment of Parkinson disease manifestations. Current Protocols in Neuroscience. , 1382-1387 (2009).
- Palmer, J. L., et al. Unified Parkinson’s Disease Rating Scale-Motor Exam: inter-rater reliability of advanced practice nurse and neurologist assessments). Journal of Advanced Nursing. 66 (6), 1382-1387 (2010).
- Neisser, U. On "Social Knowing". Personality and Social Psychology Bulletin. 6 (4), 601-604 (1980).
- Neisser, U. . Memory Observed: Remembering in Natural Contexts. , (1982).
- Jekel, K., et al. Mild cognitive impairment and deficits in instrumental activities of daily living: a systematic review. Alzheimer’s Research & Therapy. 7 (1), 17 (2015).
- Chisholm, D., Toto, P., Raina, K., Holm, M., Rogers, J. Evaluating capacity to live independently and safely in the community: Performance assessment of self-care skills. British Journal of Occupational Therapy. 77 (2), 59-63 (2014).
- Cipresso, P., et al. Virtual multiple errands test (VMET): a virtual reality-based tool to detect early executive functions deficit in Parkinson’s disease. Frontiers in Behavioral Neuroscience. 8, 405 (2014).
- Owsley, C., Sloane, M., McGwin, G., Ball, K. Timed instrumental activities of daily living tasks: relationship to cognitive function and everyday performance assessments in older adults. Gerontology. 48 (4), 254-265 (2002).
- Brennan, L., et al. The Penn Parkinson’s Daily Activities Questionnaire-15: Psychometric properties of a brief assessment of cognitive instrumental activities of daily living in Parkinson’s disease. Parkinsonism & Related Disorders. 25, 21-26 (2016).
- Arlati, S., et al. Acceptance and usability of immersive virtual reality in older adults with objective and subjective cognitive decline. Journal of Alzheimer’s Disease. 80 (3), 1025-1038 (2021).
- Porffy, L. A., et al. A novel virtual reality assessment of functional cognition: validation study. Journal of Medical Internet Research. 24 (1), 27641 (2022).
- Swanson, C. W., Fling, B. W. Discriminative mobility characteristics between neurotypical young, middle-aged, and older adults using wireless inertial sensors. Sensors. 21 (19), 6644 (2021).
- Yeh, T. T., Liang, P. J., Lee, S. C. Differences in walking-to-turning characteristics between older adult fallers and nonfallers: a prospective and observational study using wearable inertial sensors. International Journal of Rehabilitation Research. 45 (1), 53-57 (2022).
- Zach, H., et al. Identifying freezing of gait in Parkinson’s disease during freezing provoking tasks using waist-mounted accelerometry. Parkinsonism & Related Disorders. 21 (11), 1362-1366 (2015).
- Bhatt, H., Pieruccini-Faria, F., Almeida, Q. J. Dynamics of turning sharpness influences freezing of gait in Parkinson’s disease. Parkinsonism & Related Disorders. 19 (2), 181-185 (2013).
- Hoops, S., et al. Validity of the MoCA and MMSE in the detection of MCI and dementia in Parkinson disease. Neurology. 73 (21), 1738-1745 (2009).
- Bruck, S., Watters, P. A. Estimating cybersickness of simulated motion using the simulator sickness questionnaire (SSQ): A controlled study. Proceedings of the 2009 Sixth International Conference on Computer Graphics, Imaging and Visualization; Institute of Electrical and Electronics Engineers (IEEE). , 486-488 (2009).
- Kennedy, R. S., Lane, N. E., Berbaum, K. S., Lilienthal, M. G. Simulator sickness questionnaire: An enhanced method for quantifying simulator sickness. The International Journal of Aviation Psychology. 3 (3), 203-220 (1993).
- Brooke, S. . Usability Evaluation in Industry. , 189-194 (1996).
- Lewis, J. R., Sauro, J. The factor structure of the system usability scale. Human Centered Design. , 94-103 (2009).
- Sauro, J., Lewis, J. R. . Quantifying the User Experience: Practical Statistics for User Research. 2nd ed. , (2016).
- Niehorster, D. C., Li, L., Lappe, M. The accuracy and precision of position and orientation tracking in the HTC Vive virtual reality system for scientific research. i-Perception. 8 (3), 2041669517708205 (2017).
- Suchy, Y., Kraybill, M. L., Franchow, E. Instrumental activities of daily living among community-dwelling older adults: discrepancies between self-report and performance are mediated by cognitive reserve. Journal of Clinical and Experimental Neuropsychology. 33 (1), 92-100 (2011).
- Reppermund, S., et al. Impairment in instrumental activities of daily living with high cognitive demand is an early marker of mild cognitive impairment: the Sydney memory and ageing study. Psychological Medicine. 43 (11), 2437-2445 (2013).
- Bangor, A., Kortum, P. T., Miller, J. T. An empirical evaluation of the system usability scale. International Journal of Human-Computer Interaction. 24 (6), 574-594 (2008).
- Kortum, P., Sorber, M. Measuring the usability of mobile applications for phones and tablets. International Journal of Human-Computer Interaction. 31 (8), 518-529 (2015).
- Alberts, J. L., et al. Development and implementation of a multi-disciplinary technology enhanced care pathway for youth and adults with concussion. Journal of Visualized Experiments. (143), e58962 (2019).
- Rhodes, J. K., et al. Multiple Sclerosis performance test: technical development and usability. Advances in Therapy. 36 (7), 1741-1755 (2019).
- Alberts, J. L., et al. A technology-enabled concussion care pathway reduces costs and enhances care. Physical Therapy. 100 (1), 136-148 (2020).
- Macaron, G., et al. Technology-enabled assessments to enhance multiple sclerosis clinical care and research. Neurology Clinical Practice. 10 (3), 222-231 (2020).
- Porter, M. E. What is value in health care. The New England Journal of Medicine. 363 (26), 2477-2481 (2010).
- Sutton, J. M., Ash, S. R., Al Makki, A., Kalakeche, R. A. A daily hospital progress note that increases physician usability of the electronic health record by facilitating a problem-oriented approach to the patient and reducing physician clerical burden. The Permanente Journal. 23, (2019).
- Maetzler, W., et al. Modernizing daily function assessment in Parkinson’s disease using capacity, perception, and performance measures. Movement Disorders. 36 (1), 76-82 (2021).
- Stephenson, D., Badawy, R., Mathur, S., Tome, M., Rochester, L. Digital progression biomarkers as novel endpoints in clinical trials: a multistakeholder perspective. Journal of Parkinson’s Disease. 11, 103-109 (2021).
- Lu, M., et al. Vision-based estimation of MDS-UPDRS Gait scores for assessing Parkinson’s Disease motor severity. Medical Image Computing and Computer-Assisted Intervention. 12263, 637-647 (2020).
- Hobert, M. A., et al. Progressive gait deficits in Parkinson’s disease: a wearable-based biannual 5-year prospective study. Frontiers in Aging Neuroscience. 11, 22 (2019).
- Thorp, J. E., Adamczyk, P. G., Ploeg, H. L., Pickett, K. A. Monitoring motor symptoms during activities of daily living in individuals with Parkinson’s disease. Frontiers in Neurology. 9, 1036 (2018).
- Shawen, N., et al. Role of data measurement characteristics in the accurate detection of Parkinson’s disease symptoms using wearable sensors. Journal of NeuroEngineering and Rehabilitation. 17 (1), 52 (2020).
- Lu, R., et al. Evaluation of wearable sensor devices in Parkinson’s disease: a review of current status and future prospects. Parkinsons Disease. 2020, 4693019 (2020).
- Ozinga, S. J., Alberts, J. L. Quantification of postural stability in older adults using mobile technology. Experimental Brain Research. 232 (12), 3861-3872 (2014).
- Ozinga, S. J., et al. Three-dimensional evaluation of postural stability in Parkinson’s disease with mobile technology. NeuroRehabilitation. 41 (1), 211-218 (2017).
- Ozinga, S. J., Linder, S. M., Alberts, J. L. Use of mobile device accelerometry to enhance evaluation of postural instability in Parkinson disease. Archives of Physical Medicine and Rehabilitation. 98 (4), 649-658 (2017).
- Ozinga, S. J., Machado, A. G., Miller Koop, M., Rosenfeldt, A. B., Alberts, J. L. Objective assessment of postural stability in Parkinson’s disease using mobile technology. Movement Disorders. 30 (9), 1214-1221 (2015).
- Maldonado-Naranjo, A., Koop, M. M., Hogue, O., Alberts, J., Machado, A. Kinematic metrics from a wireless stylus quantify tremor and bradykinesia in Parkinson’s disease. Parkinson’s Disease. 2019, 6850478 (2019).
- Lingaiah, A., et al. Improving anxiety in Parkinson’s disease: A cautionary tale about mobile health technologies. Parkinsonism & Related Disorders. 73, 50-51 (2020).
- di Biase, L., et al. Quantitative analysis of bradykinesia and rigidity in Parkinson’s disease. Frontiers in Neurology. 9, 121 (2018).
- Espay, A. J., et al. Technology in Parkinson’s disease: Challenges and opportunities. Movement Disorders. 31 (9), 1272-1282 (2016).
- Sieber, B. A., et al. Prioritized research recommendations from the National Institute of Neurological Disorders and Stroke Parkinson’s Disease 2014 conference. Annals of Neurology. 76 (4), 469-472 (2014).
- van Uem, J. M., et al. Health-related quality of life in patients with Parkinson’s disease–A systematic review based on the ICF model. Neuroscience & Biobehavioral Reviews. 61, 26-34 (2016).
- Papadopoulos, E., Buracchio, T. Drug Development Tool (DDT) COA #000142. U.S. Food & Drug Administration. , (2021).

