14.9:
勒夏特列原理(LeChatelier's Principle) :温度变化
Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
JoVE Core
Kimya
Le Chatelier’s Principle: Changing Temperature
温度会影响化学反应的速率;因此,对于一个平衡状态下的 反应,温度的变化对体系起着应力的作用。勒沙特列原理预测了系统将如何 响应,以最小化此类干扰。温度的变化会改变 平衡常数的值,这与浓度或体积的变化不同,它会移动平衡而不会改变 K 的值。考虑一下将气态五氯化磷分解为 三氯化磷和氯气气体的反应。对于这种吸热反应,吸收的热量 可以看作是一种反应物。温度的升高会给体系增加 热量,类似于添加更多的一种反应物。因此,平衡位置向产物移动,产生更多的三氯化磷和氯气 来消耗额外的热量,因为 平衡常数 K 的值增加了。另一方面,温度的降低 会从体系中带走热量,类似于除去一种反应物。平衡位置向反应物移动,产生更多的五氯化磷 来释放热量,因为 K 的值降低了。对于放热反应,例如二氧化硫和氧气 之间的气体反应 生成三氧化硫,释放的热量 可以看作是一种产物。温度的升高类似于添加 更多的一种产物。这会导致平衡位置 向反应物移动,产生更多的二氧化硫 和氧气来吸收一些额外的热量,因为 K 值降低了。相反地,降低这个放热反应 的温度会带走热量,就像除去一种产物一样。平衡位置向产物移动,产生更多的三氧化硫以释放热量,因为 K 增加了。因此,温度升高有利于 吸热反应中的产物,而温度降低 有利于放热反应中 的产物。
14.9:
勒夏特列原理(LeChatelier's Principle) :温度变化
与质量作用定律一致,浓度变化所强调的平衡将转变为重新建立平衡,而不会改变平衡常数的值, K。 当平衡因温度变化而变化时, 然而,它以不同的相对成分重新建立,显示了平衡常数的不同值。
要了解这种现象,请考虑基本反应:
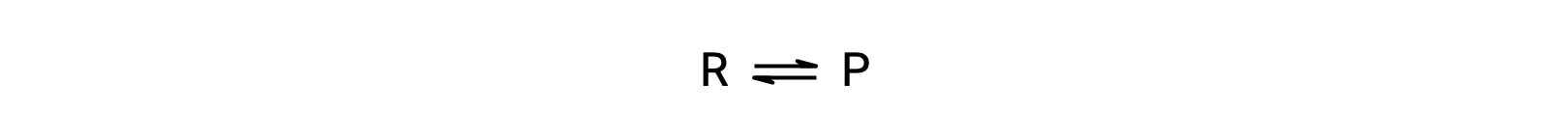
由于这是一种基本反应,正向和反向的速率定律可以直接从平衡方程的化学计量法中得出:
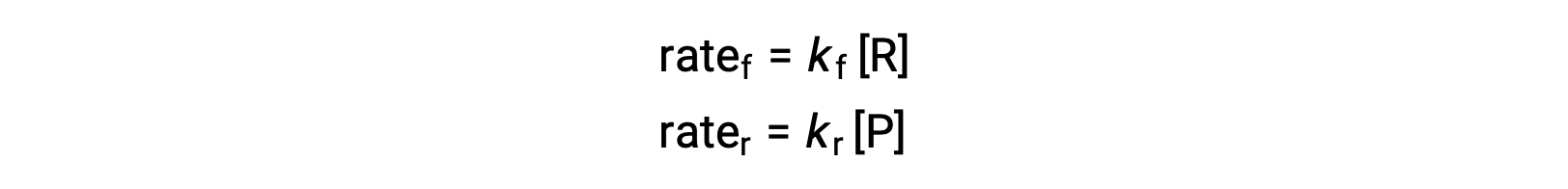
当系统处于平衡状态时,
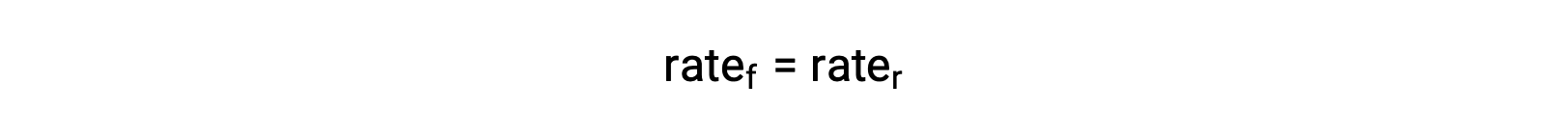
将速率定律替换为这一相等,并重新排列
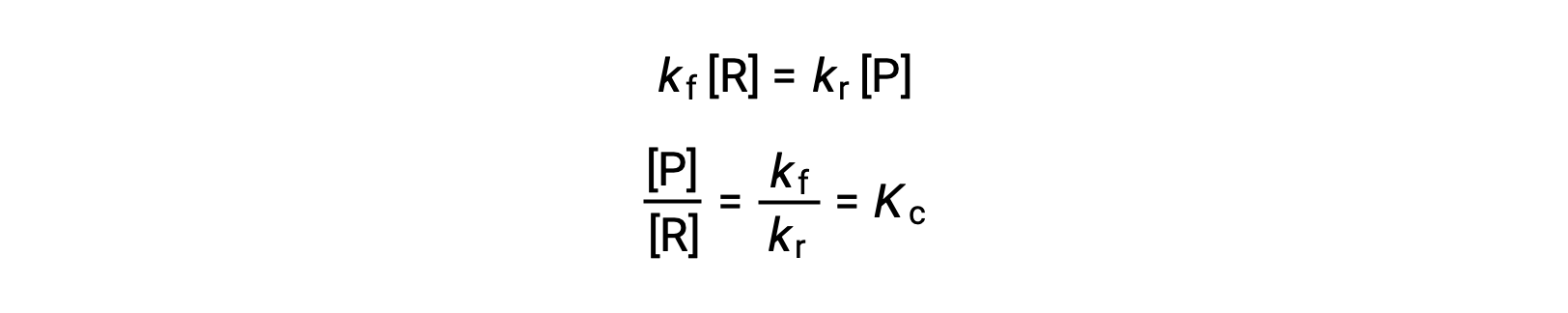
平衡常数可以表示为正向和反向反应的率值常量的数学函数。 由于率值常量随阿伦尼乌斯方程所述的温度而变化,因此平衡常量也会随温度变化而变化 (假设率值常量受温度变化影响到不同范围)。 对于涉及多步反应机理的更复杂的反应,率值中步骤的平衡常数和机理常数之间存在类似但更复杂的数学关系。 无论反应的复杂程度如何,其平衡常数的温度依赖性仍然存在。
通过考虑到反应的焓变化,最方便的方法是预测温度变化时的平衡。 例如, Haber 过程产生的氨是放热 (热产生) 过程:
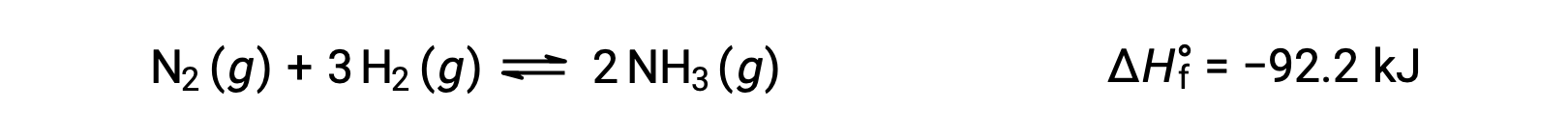
为了应用 勒夏特列原理(Le Chatelier’s Principle) , 热 , q 可以被视为生成物:
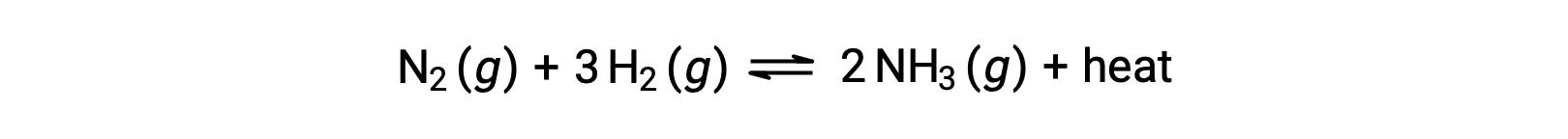
升高系统温度就像增加生成物的数量一样,因此平衡将向左移动。 降低系统温度同样会导致平衡向右移动。 对于吸热过程,热量被视为反应的反应物,因此观察到相反的温度依赖性。
本文改编自 Openstax, 化学 2e, 第13.3节:平衡位移: Le Châtelier ’ s principle。
