13.3:
농도와 속도 법칙
13.3:
농도와 속도 법칙
반응의 비율은 반응의 농도에 의해 영향을 받습니다. 속도법(차등율법) 또는 금리 방정식은 화학 반응의 속도와 반응의 농도 사이의 관계를 설명하는 수학적 표현입니다.
예를 들어, 일반적인 반응A+ bB ~ B ∞ 제품, 여기서 a와 b는 stoichiometric 계수, 속도 법은 다음과 같이 작성될 수 있습니다:
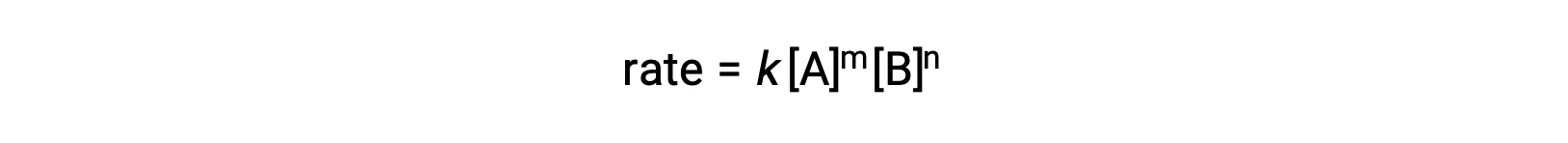
[A] 및 [B]는 반응제의 어금니 농도를 나타내며, K는 특정 온도에서 특정 반응에 특이적인 속도 상수이다.
지수 m과 n은 반응 순서이며 일반적으로 긍정적 인 정수이지만 분획, 음수 또는 0일 수 있습니다.
속도 상수 k및 반응 주문 m 및 n은 반응의 농도가 변화함에 따라 반응 속도가 어떻게 변하는지 관찰함으로써 실험적으로 결정된다. 속도 상수 k는 반응성 농도와 는 무관하지만 온도에 따라 다릅니다.
속도 법의 반응 명령은 반응 성 농도에 대한 비율의 수학적 의존성을 설명합니다. 일반요율법(속도 =k[A]m[B]n)을참조하여, B에 대하여 A 및 n 주문에 대하여 반응은 m 순서이다. 예를 들어 m = 1 및 n = 2인 경우 반응은 B의 A 및 두 번째 순서로 첫 번째 순서입니다. 전체 반응 순서는 단순히 각 반응에 대한 주문의 합계입니다. 여기서 실시율법에 대해 반응은 전체 3차(1 + 2 = 3)이다.
금리법 결정에 대한 일반적인 실험적 접근 방식은 초기 금리의 방법입니다. 이 방법은 다른 초기 반응성 농도를 사용하여 수행 된 다중 실험 시험에 대한 반응 속도를 측정하는 것을 포함한다. 이러한 시험에 대한 측정 된 비율을 비교하면 반응 명령의 결정이 허용되며, 그 후 속도상수는 비율 법을 공식화하는 데 사용됩니다.
요금법은 일부 반응제에 대해 분수 명령을 나타낼 수 있으며, 반응율이 증가할 경우 부정적인 반응 순서가 관찰되기도 한다. 속도 법은 실험에 의해서만 결정되며 반응 에 의해 안정적으로 예측되지 않는다는 점에 유의하는 것이 중요합니다.
반응 순서는 반응 속도와 반응물질 또는 제품의 농도 사이의 관계를 결정한다.
• 제로 오더 반응에서, 반응의 농도는 전체적으로 일정하게 유지 반응의 속도에 영향을 미치지 않습니다.
• 1차 반응에서 반응 속도는 반응성 농도의 변화에 직접적이고 선형적으로 비례합니다. 반응성 농도가 감소함에 따라 반응속도도 비례적으로 감소합니다.
• 2차 또는 고차 반응에서 반응 속도는 반응자의 기하급수적 가치에 비례합니다. 따라서 반응이 진행되고 반응의 농도가 감소함에 따라 반응 속도가 기하급수적으로 감소합니다.
