18.9:
부식
18.9:
부식
자연 전기 화학 공정으로 인한 금속의 분해는 부식이라고합니다. 철에 녹 형성, 은의 변색, 구리에 발생하는 블루 그린 파티나 부식의 예입니다. 부식은 금속의 산화를 포함한다. 때로는 구리 또는 알루미늄의 산화와 같은 보호, 금속 산화물의 보호 층 또는 그 유도체가 표면에 형성되어 기본 금속을 추가 산화로부터 보호합니다. 다른 경우에는, 부식은 철의 녹슨 것과 같은 금속에 손상을 입힙니다.
바람직하지 않은 레독스 반응 : 철의 녹슬기
녹슬은 산소와 물에 철의 노출로 인해 발생합니다. 녹 형성은 철의 표면에 갈바닉 세포의 생성을 포함, 이는 철의 생성을 초래 (II). 철 표면에 형성된 무심(철산화) 및 음극(산소 의 감소) 부위에서 발생하는 관련 레독스 반응은 다음과 같습니다.
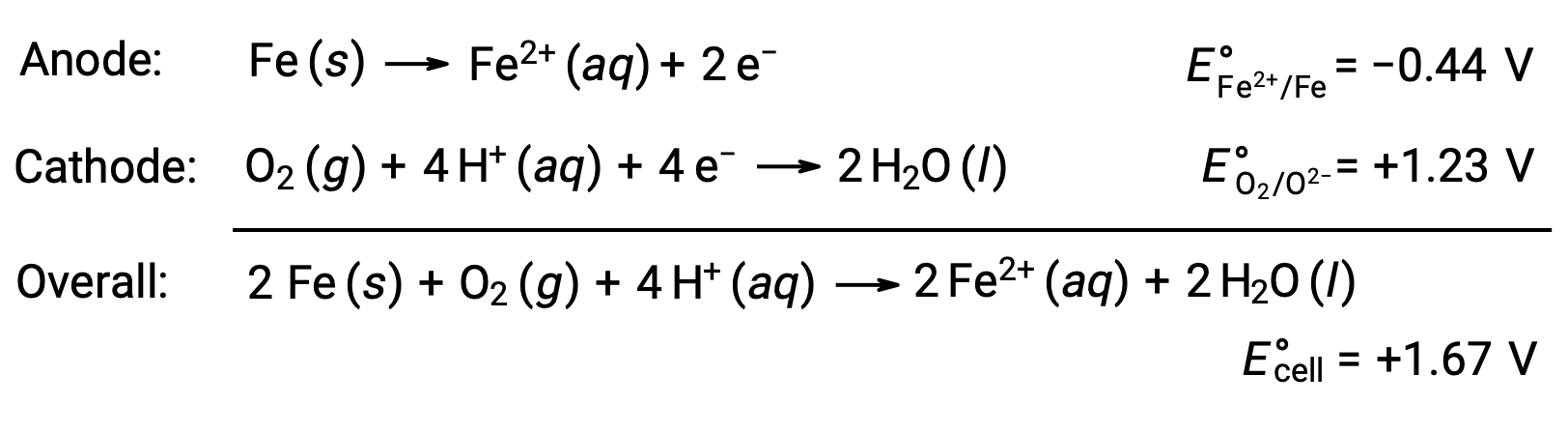
철분(II)은 습한 공기와 더 반응하여 일반적으로 녹으로 알려진 철(III) 산화물 수분을 형성합니다.
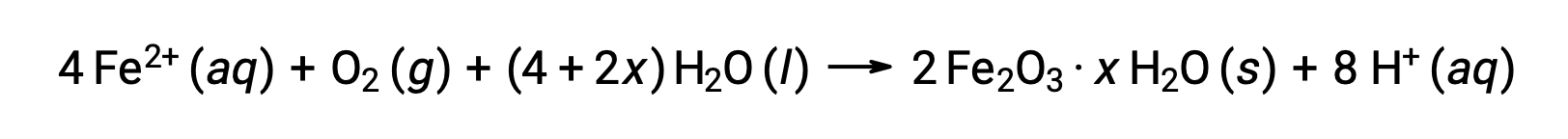
수화물의 stoichiometry는 화합물 포뮬러에서 x의 사용에 의해 표시된 바와 같이 철(II)이 노출되는 물의 양에 따라 다릅니다. 수분, 산과 전해질의 존재는 녹의 형성 속도를 증가시킵니다. 구리의 파티나와 는 달리 녹의 형성은 보호층을 생성하지 못하므로 녹이 벗겨지고 대기에 신선한 철을 노출함에 따라 철의 부식이 계속됩니다.
부식 방지
부식을 방지하기 위해 다양한 방법을 사용할 수 있습니다. 한 가지 방법은 물과 산소와의 접촉을 피하기 위해 금속 표면을 페인트로 칠하는 것입니다. 스테인레스 스틸에 소량의 크롬과 철을 혼합하는 것과 같은 금속합금은 부식을 방지하는 또 다른 효과적인 방법입니다. 크롬은 표면 근처에서 수집되어 산화를 거치므로 철을 부식으로부터 효과적으로 보호합니다.
철및 기타 금속은 아연에 의해 부식으로부터 보호될 수 있으며, 보호되는 금속은 일반적으로 아연을 보다 쉽게 산화된 금속층으로 코팅하는 공정이다. 아연 층이 손상되지 않은 경우 공기가 기본 철에 닿지 않도록 하여 부식을 방지합니다. 아연 층이 부식 또는 기계적 마모에 의해 침해되는 경우, 철은 다음 단락에 설명된 음극 보호 프로세스에 의해 부식으로부터 보호될 수 있습니다.
음극 보호는 전기 화학 반응에서 음극으로 보호되는 금속을 변환하는 원리를 활용합니다. 이는 보호된 금속을 희생 양극으로 알려진 아연 이나 마그네슘과 같은 보다 활성또는 쉽게 산화된 금속에 연결함으로써 달성된다. 양극은 부식되어 음극 역할을하는 금속을 보호하는 데 사용됩니다. 음극 보호는 온수기 및 지하 수납 탱크와 같은 가전 제품에 가장 일반적으로 사용됩니다. 중요한 것은, 음극 보호는 철 이외의 금속에 사용할 수 있습니다.
이 텍스트는 OpenStax, 화학 2e, 제 17.6 장: 부식에서채택됩니다.
