Informação estrutural de uma única molécula de FRET experimentos usando a Nano-posicionamento sistema rápido
Summary
We present the setup and experimental procedure to obtain smFRET data from large donor-acceptor networks with a TIRF microscope. The step-by-step analysis of these measurements with the Bayesian inference software Fast-NPS yields high-resolved structural information via the application of adapted dye models.
Abstract
Single-molecule Förster Resonance Energy Transfer (smFRET) can be used to obtain structural information on biomolecular complexes in real-time. Thereby, multiple smFRET measurements are used to localize an unknown dye position inside a protein complex by means of trilateration. In order to obtain quantitative information, the Nano-Positioning System (NPS) uses probabilistic data analysis to combine structural information from X-ray crystallography with single-molecule fluorescence data to calculate not only the most probable position but the complete three-dimensional probability distribution, termed posterior, which indicates the experimental uncertainty. The concept was generalized for the analysis of smFRET networks containing numerous dye molecules. The latest version of NPS, Fast-NPS, features a new algorithm using Bayesian parameter estimation based on Markov Chain Monte Carlo sampling and parallel tempering that allows for the analysis of large smFRET networks in a comparably short time. Moreover, Fast-NPS allows the calculation of the posterior by choosing one of five different models for each dye, that account for the different spatial and orientational behavior exhibited by the dye molecules due to their local environment.
Here we present a detailed protocol for obtaining smFRET data and applying the Fast-NPS. We provide detailed instructions for the acquisition of the three input parameters of Fast-NPS: the smFRET values, as well as the quantum yield and anisotropy of the dye molecules. Recently, the NPS has been used to elucidate the architecture of an archaeal open promotor complex. This data is used to demonstrate the influence of the five different dye models on the posterior distribution.
Introduction
A determinação da estrutura de uma biomolécula é um pré-requisito fundamental para a compreensão da sua função. Dois métodos bem estabelecidos para a determinação da estrutura são microscopia de elétrons crio e cristalografia de raios X 1, 2. Hoje em dia, ambos os métodos proporcionam informação estrutural de alta resolução com uma resolução até o nível Angstrom. Estes dois métodos têm sido utilizados extensivamente para elucidar a estrutura de biomoléculas grandes, tais como complexos de proteína. Embora os métodos existentes têm sido constantemente melhorado ao longo das últimas décadas, a complexidade das estruturas biológicas ainda representa um grande desafio para a biologia estrutural, especialmente quando grandes complexos, dinâmicos e transitórios são investigados 3.
A fim de estudar a dinâmica dos complexos macromoleculares ea relação estrutura-função em particular, metodologias de molécula única tem provinformações úteis ided 4. Várias novas estratégias foram desenvolvidas fornecendo uma abordagem ortogonal sobre a aquisição de informação estrutural e dinâmica. Exemplos são de alta velocidade AFM 5, 6 manipulação mecânica, microscopia de fluorescência localização 7, bem como uma única molécula de Transferência de Energia de Ressonância de Förster (smFRET) 8, 9. Desde muito cedo na FRET tem sido denominado uma régua molecular, devido à distância a dependência na escala de comprimento de 10 biomacromoléculas.
Uma aplicação particularmente interessante do smFRET é usar a informação obtida a partir de medições de distância smFRET inferir estrutural informações 11, 12, 13, 14, 15 </sup>, 16, 17, 18, 19, 20, 21, 22, 23. Devido à elevada resolução de tempo de smFRET, a posição dos elementos móveis de uma estrutura de proteína pode ser localizada. No entanto, a fim de extrair a informação quantitativa a partir de dados smFRET importantes parâmetros de correcção sobre as moléculas de corante precisa de ser determinada durante a medição 24. Com estes factores de correcção, a eficiência de FRET FRET E pode ser calculado usando a fórmula
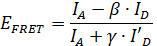 ,
,
onde A e I D </sUB> são as intensidades de fluorescência do dador e do aceitador molécula, respectivamente (ver Figura 2). O fator β representa cross-talk, a fuga de emissões de doadores para o canal receptor e é calculado

onde eu A e I 'D são as intensidades de fluorescência do dador e da molécula receptora após a foto branqueamento da molécula receptora.
O factor γ corrige a diferença nas eficiências de detecção em relação nos dois canais, bem como as diferenças no rendimento quântico de fluorescência do dador e o corante aceitador. É calculado de cada traço do tempo individual,
<p class="jove_content" fo:keep-together.within-page="1" fo:text-align="center" style = "text-align: center;">
Note-se, que esta descrição negligencia excitação directa da molécula aceitadora, que por vezes se torna importante e que seria necessário para ser corrigido para assim. Para determinar esses fatores de correção é útil para excitar tanto o doador, bem como o receptor em um esquema de alternância 25, a fim de diferenciar entre mudanças foto-física e dinâmica estrutural.
A fim de não só obter eficiências smFRET quantitativos, mas também informações sobre a estrutura quantitativa, o Sistema de Nano-Posicionamento (NPS) foi introduzido em 2008 26. O nome foi escolhido com base nas suas semelhanças com o sistema de posicionamento global por satélite (GPS). O NPS é uma técnica híbrida que combina smFRET e os dados de cristalografia de raios-X para a localização de posições de corante desconhecidos em complexos biomacromolecular. O Crystal estrutura serve como uma armação de referência e os resultados smFRET são utilizadas para obter informação sobre a distância entre uma posição desconhecido fluoróforo (antena) e uma posição conhecida a partir da estrutura cristalina (satélite). Em experiências consecutivas as distâncias entre a antena e vários satélites são medidos e a posição da antena é determinada por meio de um esquema de análise estatística rigorosa com base na estimativa de parâmetros Bayesiano. Como resultado, não só a posição mais provável da antena é calculado, mas a sua distribuição incerteza 3D completa, a chamada posterior, visualizado por volumes credíveis. Além disso, o NPS foi expandido para permitir a análise de redes atinjam 27 smFRET.
O NPS tem sido utilizado para resolver um certo número de questões importantes na transcrição eucariótica, ou seja, o curso do ADN a montante, o DNA não-molde e o ARNm nascente no co alongamento de ARN polimerase IImplex 12, 28, também demonstra o efeito de factores de iniciação da transcrição 26 e a arquitectura dinâmico de um promotor-aberto complexo 29. Além disso, o NPS foi usada para elucidar a estrutura do complexo de archaea aberta de ARN polimerase 30 e, em particular, a posição de início de transcrição factor de TFE, que se liga competitivamente ao mesmo local como o factor de alongamento da transcrição Spt4 / 5 31.
Desde então, uma série de abordagens baseadas smFRET estruturais foram publicados 15, 18, 21, 23. Ao comparar diferentes métodos baseados smFRET estruturais, torna-se claro que a aparente precisão do método é altamente dependente da escolha particular de modelos de corante. Note-se quemoléculas de corante pode apresentar um comportamento espacial e de orientação diferente, dependendo do seu ambiente local.
Para este fim, Fast-NPS foi introduzido 32. Fast-NPS usa um algoritmo de amostragem avançada reduzindo os tempos de cálculo drasticamente. Além disso, o NPS-rápida permite a realização de uma análise estrutural e para cada molécula de corante o utilizador pode escolher a partir de um conjunto de cinco modelos diferentes de corante, que serão descritos a seguir. O modelo mais conservador, chamado de clássico, assume que o corante ocupa apenas um, mas desconhecida, posição. Nesta posição, o fluoróforo pode rodar livremente no interior de um cone, cujo tamanho é determinado a partir do seu respectivo anisotropia de fluorescência (dependente do tempo). A orientação do cone não é conhecida, o que conduz a grandes incertezas na conversão eficiências smFRET medidos em distâncias. A este respeito, é o modelo conservador, uma vez que irá conduzir à menor precisão em comparação com o outro modo de corantels. Somente para distâncias muito curtas caso as suposições feitas pelo modelo de liderança clássico para a determinação da posição visivelmente incorreto. Para valores smFRET típicos, a posição correta é sempre incluído no comparativamente grande volume credível.
No entanto, uma vez que uma maior precisão é desejável, é importante para desenvolver e testar modelos de corantes alternativos, que poderiam ajudar a melhorar a precisão. Se o corante gira muito mais rápido do que o seu tempo de vida de fluorescência inerente, o assim chamado modelo ISO pode ser aplicada. Aqui, o factor de orientação de K 2 (necessária para o cálculo do raio Förster isotrópico característica  ) Está definido para 2/3. Como resultado, os volumes são calculados credíveis quase duas ordens de grandeza menor, em comparação com aqueles no modelo clássico 32. No caso em que o fluoróforo é encontrada num ambiente que permite não só reori rápidoentação, mas o movimento adicionalmente rapidamente em todo o seu volume acessível, deve ser utilizado o modelo meanpos-iso. Neste modelo, o corante ocupa efetivamente apenas uma posição média, onde a média espacial é representada por uma conversão de distância polinomial 15. Este modelo aplica-se, por exemplo, a (geralmente hidrofóbico) corante está ligado a uma região hidrofílica, por exemplo, o ADN. Aplicação do modelo meanpos-iso leva a uma redução adicional do tamanho dos volumes credíveis por um factor de aproximadamente dois. No entanto, um corante ligado a uma proteína pode ligar-se reversivelmente a várias manchas hidrofóbicas em seu volume estericamente acessíveis (AV). Um fluoróforo que instantaneamente alterna entre essas regiões, mas dentro de uma região sofre livre rotação e movimento rápido localizado é melhor descrito pelo modelo VAR-meanpos-iso. Para uma situação semelhante em que o corante não é livre para girar VAR-meanpos modelo se aplica. Mais d etails sobre esses modelos podem ser encontrados em nossa recente publicação 32.
) Está definido para 2/3. Como resultado, os volumes são calculados credíveis quase duas ordens de grandeza menor, em comparação com aqueles no modelo clássico 32. No caso em que o fluoróforo é encontrada num ambiente que permite não só reori rápidoentação, mas o movimento adicionalmente rapidamente em todo o seu volume acessível, deve ser utilizado o modelo meanpos-iso. Neste modelo, o corante ocupa efetivamente apenas uma posição média, onde a média espacial é representada por uma conversão de distância polinomial 15. Este modelo aplica-se, por exemplo, a (geralmente hidrofóbico) corante está ligado a uma região hidrofílica, por exemplo, o ADN. Aplicação do modelo meanpos-iso leva a uma redução adicional do tamanho dos volumes credíveis por um factor de aproximadamente dois. No entanto, um corante ligado a uma proteína pode ligar-se reversivelmente a várias manchas hidrofóbicas em seu volume estericamente acessíveis (AV). Um fluoróforo que instantaneamente alterna entre essas regiões, mas dentro de uma região sofre livre rotação e movimento rápido localizado é melhor descrito pelo modelo VAR-meanpos-iso. Para uma situação semelhante em que o corante não é livre para girar VAR-meanpos modelo se aplica. Mais d etails sobre esses modelos podem ser encontrados em nossa recente publicação 32.
Estes modelos oferecem um extenso repertório de explicar especificamente para os diversos ambientes de um corante pode encontrar e aplicá-las com sabedoria otimiza sua precisão de localização. Em Fast-NPS cada molécula corante ligado a uma posição específica pode ser atribuído a um modelo individual, de modo que Fricção-parceiros são autorizados a ter modelos diferentes. Isto permite a modelagem ilimitadas e próxima do natureza. No entanto, é importante que uma executa testes estatísticos rigorosas para assegurar que o resultado obtido pela combinação modelo final ainda está em concordância com os dados experimentais. Estes testes são incluídos no software Fast-NPS.
A fim de aplicar Fast-NPS para dados experimentais é requerida a medição de (apenas) de três parâmetros de entrada. Em primeiro lugar, o corante de par isotrópico Förster específica raios (/54782/54782eq5.jpg "/>) Têm de ser determinados. Portanto, o rendimento quântico (QY) do corante dador, os espectros de emissão de fluorescência de dador e absorção de aceitador os espectros têm de ser medidos. Essas medições podem ser efectuadas em grandes quantidades, usando um espectrómetro de padrão e um espectrómetro de fluorescência padrão. Para cada par, a R 0 é, então, calculado usando a PhotochemCAD gratuito e pode ser usado na análise de NPS. Além disso, as (tempo-resolvido) anisotropias de fluorescência das moléculas de corante precisa para ser obtido usando uma polarização (e tempo) sensível espectrômetro de fluorescência. no entanto, os parâmetros de entrada mais importantes para fast-NPS são as eficiências smFRET medidos em uma configuração de microscopia de fluorescência única molécula, tais como um total microscópio reflexão interna de fluorescência (TIRFM) .
Aqui, apresentamos um protocolo passo-a-passo para a obtenção de dados smFRET e aplicando Fast-NPS (Figura 1).
Protocol
Representative Results
Discussion
Apresenta-se o procedimento de instalação e experimental para determinar com precisão a eficiência FRET entre corantes ligados através de elementos de ligação flexíveis a biomacromoléculas, ou seja, ácidos nucleicos e / ou proteínas.
A fim de assegurar medições precisas smFRET (secção 3), que é fundamental para excluir o ar da câmara de fluxo em qualquer momento durante a medição. Além disso, certifique-se de não sobrecarregar a câmara de fluxo com fluoróforos. Os fluoróforos devem ser claramente separadas para garantir a análise correta. Como pares smFRET, que não apresentam branqueamento do doador tem que ser excluídos da análise, certifique-se de que> 80% das moléculas no campo de visão são branqueados no final do filme. Para ter em conta não homogeneidades na amostra do factor-β e o factor γ, corrigindo os cross-talk e relativas eficiências de detecção do canal de dador e aceitador, respectivamente, são calculados para cada par de FRET individualmente.
<p class= "Jove_content"> As definições da câmara (tempo de integração, ganho de multiplicador de elétrons, ganho pré-amplificador e taxa de leitura descrito na Seção 3.9) deve ser definido para valores que dão o melhor equilíbrio entre a relação sinal-ruído, gama dinâmica e tempo-resolução. Eles precisam ser reajustado para diferentes experimentos ou se hardware diferente é usado. Os números de quadros precisa de ser suficientemente elevada para assegurar que a maior parte do doador moléculas lixívia dentro do período de observação.Para as medições sobre o espectrômetro de fluorescência (Secções 7 a 9) um bom compromisso entre a intensidade do sinal ea resolução espectral dos dados gravados tem de ser encontrada. Para este efeito, as fendas na via de excitação e emissão do espectrómetro de fluorescência têm de ser adaptados dependendo do instrumento usado e a concentração da amostra.
Além disso, apresentamos o método de análise Fast-NPS para obter informações estrutural da MACROM transitória ou dinâmicocomplexos olecular. NPS foi aplicado para revelar o caminho do filamento de DNA não-molde e a posição dos factores de iniciação de transcrição no complexo aberta de ARN-polimerase de archaea. Usando a rede de mais de 60 medições de distâncias diferentes, mostramos que a Fast-NPS, equipado com um motor de amostragem recém-implementado (Eilert, T., Beckers, M., Drechsler, F., & Michaelis, J. em preparação), reduz o tempo necessário para a análise desta rede smFRET complexo por ≈2 ordens de grandeza, em comparação com o método de NPS global original 27. a robustez do algoritmo está enraizada em um sampler Metropolis-dentro-Gibbs combinada com um esquema de têmpera paralelo. Fast-NPS mostra reprodutibilidade exata dos resultados da rede e é consistente com os resultados publicados anteriormente 30.
Vários métodos diferentes foram publicados com o objetivo de inferir informações estruturais a partir de medições smFRET 11 </sup>, 12, 13, 14, 15, 16, 17, 18. Todas estas abordagens fornecem apenas um modelo de corante específico. Assim, corantes, que não cumprem as suposições feitas pelo respectivo modelo, não pode ser usado ou levar a informações estruturais falsa. Fast-NPS, pelo contrário, permite seleccionar para cada molécula de corante de um modelo diferente. Isto ajuda a explicar diferente comportamento conformacional de ambas, a molécula de corante em si, bem como o ligante utilizado para a sua fixação. Os arredores moleculares locais da molécula do corante, bem como as suas propriedades físicas vai determinar qual o modelo que é mais adequada.
Para a rede smFRET analisados do complexo de iniciação de archaea, um pressuposto isotrópica para todas as moléculas de corante conduz a uma diminuição drástica in o tamanho dos volumes credíveis, em comparação com o modelo clássico. Em combinação com uma dinâmica posição média para todas as moléculas de corante da mediana de todos os tamanhos de volume credíveis (a 95%) reduz-se a menos de 0,5 Nm 3. No entanto, estes traseiros molécula corante já não são consistentes com suas medidas smFRET, indicando que as suposições feitas levam a informação estrutural falsa. Em contraste, os posteriores determinados no modelo clássico são consistentes com as eficiências smFRET determinados.
Como o pressuposto de posição isotrópico e / ou dinâmico de uma média de todos os corantes levar a inconsistências, Fast-NPS permite antecedentes molécula do corante em que cada corante pode ser atribuída uma das cinco modelos. Cada modelo usa o mesmo volume acessível. O algoritmo para o cálculo dos AVs corante faz várias suposições. Na primeira, forma espacial do fluoróforo é aproximada por uma esfera. Assim, um diâmetro tendo em conta wid do fluoróforoth, altura e espessura deve ser utilizado (Seção 12). Além disso, a forma do ligante é aproximada por uma haste flexível. Os valores apresentados na Secção 12, foram calculados para o corante Alexa 647 ligado por via de um ligante de 12-C. Até à data, não é possível determinar com exactidão, a priori, qual o modelo mais adequado, dada a geometria experimental, e, portanto, todos os modelos devem ser testados. Em geral, uma irá escolher o modelo que dá o menor tamanho possível posterior, enquanto continua a ser consistente com os dados. Para testar se uma escolha de modelos é consistente com os dados smFRET, calcula-se tanto a parte posterior e a probabilidade. Consistência significa que mais de 90% das amostras recolhidas a partir da posterior estão dentro do intervalo de confiança de 95% da probabilidade.
Embora seja verdade que quanto menor a anisotropia, quanto menor for a distância incerteza, numa rede smFRET disposições geométricas das moléculas de corante também tem que ser tida em conta. Assim, enquanto Representing moléculas de corante com uma baixa anisotropia de fluorescência com um modelo de iso é uma primeira escolha típica, o teste de consistência fornece um meio mais diretas para a escolha do modelo de corante correta. A escolha óptima de modelos de corante podem conduzir a um aumento drástico na precisão de localização e, ao mesmo tempo, manter a consistência da rede com os seus dados de FRET.
Para resumir, Fast-NPS permite obter informações sobre a estrutura e dinâmica dos grandes complexos macromoleculares. Em contraste com os métodos estruturais comuns, tais como cristalografia de raios-X ou microscopia electrónica de crio este permite o monitoramento complexos altamente flexíveis ou transientes, assim aumentando grandemente o nosso entendimento mecanicista de processos biológicos complexos.
Disclosures
The authors have nothing to disclose.
Acknowledgements
The authors thank B. Gruchmann for the mechanical drawings of the flow chamber. Further, we want to express our gratitude to Max Beckers and Florian Drechsler for insightful comments and discussions regarding NPS and the underlying sampling engine.
Materials
| Flowchamber preparation | |||
| Customized metall sample holder | self-built | n/a | |
| quartz-glass slides, 76 x 26 mm | Technical Glass Products | 26007 | |
| coverslips, 60 x 24 mm | Marienfeld | 101242 | |
| detergent, Hellmanex II | Hellma | 320.001 | |
| ultra-pure water from Synergy UV | Millipore | 2512600 | |
| Zepto plasma cleaner | Diener | n/a | |
| (3-aminopropyl)-triethoxysilane, p.a. | Sigma-Aldrich | A3648 | |
| methoxy PEG-succinimidyl valerate, 5 kDa | Laysan Bio Inc. | MPEG-SVA-5000-1g | |
| biotinylated PEG-succinimidyl valerate, 5 kDa | Laysan Bio Inc. | BIOTIN-PEG-SVA-5000 | |
| Sodium biocarbonate | Sigma-Aldrich | S5761 Sigma | |
| Sodium carbonate | Sigma-Aldrich | S2127 Sigma-Aldrich | |
| sealing film (Nescofilm) | Fisher Scientific | 12981805 | |
| Tygon Flexible Silicone Tubing, 0.8 mm ID, 2.4 mm OD | Saint-Gobain Performance Plastics | 720958 | |
| Fine-Bore Polyethylene Tubing, 0.58 mm ID, 0.96 mm OD (Smiths Medical) | Fisher Scientific | 12665497 | |
| Neutravidin | Life Technologies | A2666 | |
| Name | Company | Catalog Number | Comments |
| Total internal reflection fluorescence microscope | |||
| Nd:YAG Laser, 532 nm | Newport Spectra-Physics | EXLSR-532-100-CDRH | |
| diode-pumped solid-state laser, 491 nm, Calypso | Cobolt | 904010050 | |
| diode laser 643 nm, iBeam smart | Toptica | iBEAM-SMART-640-S | |
| dichroic mirror, 532 RDC | Chroma | F33-540 | |
| dichroic mirror, 476 RDC | Chroma | F33-476z | |
| acousto-optic tunable filter | AA Opto-Electronic | AOTFnC-VIS | |
| plano-convex cylindrical lens, f = 75 mm | Thorlabs | LJ1703L1-A | |
| plano-concave cylindrical, f = -300 mm | Thorlabs | ||
| prism, PS 991 | Thorlabs | PS991 | |
| focussing lens, f = 75 mm | Thorlabs | LA1608-B | |
| syringe pump, PHD 2000 | Harvard Apparatus | 70-2002 | |
| 2 stepper motors, Z812B | Thorlabs | Z812B | |
| piezoelectric actuator, PE4 | Thorlabs | PE4 | |
| IR diode laser | Edmund Optics | CPS808 | part of the autofocus system |
| dichroic mirror, 775 DCXR | Chroma | 775 DCXR | |
| position-sensing detector (PSD), PDP90A | Thorlabs | PDP90A | part of the autofocus system |
| water-immersion objective, Plan Apo 60X WI, NA 1.2 | Nikon | MRD07601 | |
| dichroic mirror, 645 DCXR | Chroma | 645 DCXR | part of the emission pathway |
| emission filter, 3RD550-510 | Omega Optical | 3RD550-510 | green channel in the emission pathway |
| emission filter, 3RD660-760 | Omega Optical | 3RD660-760 | red channel in the emission pathway |
| EMCCD camera, iXon+ DU897EBV | Andor | AND-20-00032 | |
| EMCCD camera, iXon3 DU897D-BV | Andor | AND-20-000141 | |
| Name | Company | Catalog Number | Comments |
| Miscellaneous | |||
| Varian 50 | Cary | UV-VIS spectrometer | |
| Fluorolog2 | SPEX | fluorescence spectrometer | |
| Solis (V4.15) | Andor | control software for the EM-CCD camera | |
| Apt user utility (V1.022) | Thorlabs | control software for the piezo-motors | |
| Norland Optical Adhesive 68 | Thorlabs | adhesive | |
| PC-AFN-0.8 Nile red | Kisker Biotech | avidin-coated fluorescent multispec beads | |
| Matlab | Mathworks | technical computing language for custon written software | |
| Origin (V9.0) | Originlab | scientific graphing and data analysis software | |
| Hellma 105-202-15-40 | Hellma | 105-202-15-40 | absorption cuvette of 1 cm path length |
| Hellma 105-251-15-40 | Hellma | 105-251-15-40 | fluorescence cuvette with 3 mm path length |
References
- Cheng, Y. Single-Particle Cryo-EM at Crystallographic Resolution. Cell. 161, 450-457 (2015).
- Garman, E. F. Developments in X-ray Crystallographic Structure Determination of Biological Macromolecules. Science. 343 (6175), 1102-1108 (2014).
- Sali, A. Outcome of the First wwPDB Hybrid/Integrative Methods Task Force Workshop. Structure. 23, 1156-1167 (2015).
- Hopfner, K. P., Michaelis, J. Mechanisms of nucleic acid translocases: lessons from structural biology and single-molecule biophysics. Curr Opin Struct Biol. 17, 87-95 (2007).
- Ando, T., Uchihashi, T., Kodera, N. High-speed AFM and applications to biomolecular systems. Annu Rev Biophys. 42, 393-414 (2013).
- Neuman, K. K. C., Nagy, A. Single-molecule force spectroscopy: optical tweezers, magnetic tweezers and atomic force microscopy. Nat Methods. 5, 491-505 (2008).
- Yildiz, A. Myosin V walks hand-over-hand: single fluorophore imaging with 1.5-nm localization. Science. 300 (5628), 2061-2065 (2003).
- Joo, C., Balci, H., Ishitsuka, Y., Buranachai, C., Ha, T. Advances in Single-Molecule Fluorescence Methods for Molecular Biology. Annu Rev Biochem. 77 (1), 51-76 (2008).
- Hohlbein, J., Craggs, T. D., Cordes, T. Alternating-laser excitation: single-molecule FRET and beyond. Chem Soc Rev. 43 (4), 1156-1171 (2014).
- Stryer, L., Haugland, R. P. Energy transfer: a spectroscopic ruler. Proc Natl Acad Sci U S A. 58 (2), 719-726 (1967).
- Rasnik, I., Myong, S., Cheng, W., Lohman, T. M., Ha, T. DNA-binding Orientation and Domain Conformation of the E. coli Rep Helicase Monomer Bound to a Partial Duplex Junction: Single-molecule Studies of Fluorescently Labeled Enzymes. J Mol Biol. 336 (2), 395-408 (2004).
- Andrecka, J. Single-molecule tracking of mRNA exiting from RNA polymerase II. Proc Natl Acad Sci U S A. 105 (1), 135-140 (2008).
- Schröder, G. F., Grubmüller, H. FRETsg: Biomolecular structure model building from multiple FRET experiments. Comput Phys Commun. 158 (3), 150-157 (2004).
- Margittai, M. Single-molecule fluorescence resonance energy transfer reveals a dynamic equilibrium between closed and open conformations of syntaxin 1. Proc Natl Acad Sci U S A. 100 (26), 15516-15521 (2003).
- Kalinin, S. A toolkit and benchmark study for FRET-restrained high-precision structural modeling. Nat Methods. 9 (12), 1218-1227 (2012).
- Choi, J. N6-methyladenosine in mRNA disrupts tRNA selection and translation-elongation dynamics. Nat Struct Mol Biol. 23 (August 2015), 110-115 (2015).
- Svensson, B. FRET-based trilateration of probes bound within functional ryanodine receptors. Biophys J. 107 (9), 2037-2048 (2014).
- Stephenson, J. D., Kenyon, J. C., Symmons, M. F., Lever, A. M. L. Characterizing 3D RNA structure by single molecule FRET. Methods. (2016), 1-11 (2016).
- Lee, N. K. Accurate FRET measurements within single diffusing biomolecules using alternating-laser excitation. Biophys J. 88 (4), 2939-2953 (2005).
- McCann, J. J., Choi, U. B., Zheng, L., Weninger, K., Bowen, M. E. Optimizing methods to recover absolute FRET efficiency from immobilized single molecules. Biophys J. 99 (3), 961-970 (2010).
- Brunger, A. T., Strop, P., Vrljic, M., Chu, S., Weninger, K. R. Three-dimensional molecular modeling with single molecule FRET. J Struct Biol. 173, 497-505 (2011).
- Schuler, B. Single-molecule FRET of protein structure and dynamics – a primer. J nanoboitechnology. 11, 1-17 (2013).
- Choi, U. B. Single-molecule FRET-derived model of the synaptotagmin 1-SNARE fusion complex. Nat Struct Mol Biol. 17 (3), 318-324 (2010).
- Dale, R. E., Eisinger, J., Blumberg, W. E. The orientational freedom of molecular probes. The orientation factor in intramolecular energy transfer. Biophys J. 26 (2), 161-193 (1979).
- Kapanidis, A. N. Alternating-laser excitation of single molecules. Acc Chem Res. 38 (7), 523-533 (2005).
- Muschielok, A. A nano-positioning system for macromolecular structural analysis. Nat Methods. 5 (11), 965-971 (2008).
- Muschielok, A., Michaelis, J. Application of the nano-positioning system to the analysis of fluorescence resonance energy transfer networks. J Phys Chem B. 115 (41), 11927-11937 (2011).
- Andrecka, J. Nano positioning system reveals the course of upstream and nontemplate DNA within the RNA polymerase ii elongation complex. Nucleic Acids Res. 37 (17), 5803-5809 (2009).
- Treutlein, B. Dynamic Architecture of a Minimal RNA Polymerase II Open Promoter Complex. Mol Cell. 46 (2), 136-146 (2012).
- Nagy, J. Complete architecture of the archaeal RNA polymerase open complex from single-molecule. FRET and NPS. Nat Commun. 6, 6161 (2015).
- Grohmann, D., et al. The Initiation Factor TFE and the Elongation Factor Spt4/5 Compete for the RNAP Clamp during Transcription Initiation and Elongation. Mol Cell. 43 (2), 263-274 (2011).
- Beckers, M., Drechsler, F., Eilert, T., Nagy, J., Michaelis, J. Quantitative structural information from single-molecule FRET. Faraday Discuss. 184, 117-129 (2015).
- Bennink, M. L. Unfolding individual nucleosomes by stretching single chromatin fibers with optical tweezers. Nat Struct Biol. 8 (7), 606-610 (2001).
- Chandradoss, S. D. Surface passivation for single-molecule protein studies. J Vis Exp. (86), e50549 (2014).
- Würth, C., Grabolle, M., Pauli, J., Spieles, M., Resch-Genger, U. Relative and absolute determination of fluorescence quantum yields of transparent samples. Nat Protoc. 8 (8), 1535-1550 (2013).
- Lakowicz, J. R. . Principles of Fluorescence Spectroscopy. , (2006).
- Korkhin, Y. Evolution of complex RNA polymerases: The complete archaeal RNA polymerase structure. PLoS Biol. 7 (5), (2009).

