Monitoraggio della funzione polmonare con la tomografia ad impedenza elettrica nell'unità di terapia intensiva
Summary
La tomografia ad impedenza elettrica è uno strumento di monitoraggio della ventilazione polmonare in tempo reale, non invasivo e privo di radiazioni. Misurando le variazioni di impedenza nel torace, può visualizzare la distribuzione dell’aria respiro per respiro. Inizialmente destinata al monitoraggio della ventilazione, la tomografia ad impedenza elettrica può anche misurare la perfusione tramite iniezione endovenosa di una soluzione salina.
Abstract
La tomografia ad impedenza elettrica (EIT) è una tecnica di imaging all’avanguardia, non invasiva e priva di radiazioni per il monitoraggio continuo e in tempo reale della ventilazione. Ha anche un’applicazione nel monitoraggio della perfusione polmonare. L’EIT quantifica i modelli di ventilazione e perfusione nel polmone dalla misurazione e dall’elaborazione delle variazioni di impedenza nel torace. È un potente strumento per i medici per visualizzare i cambiamenti respiro per respiro nella funzione polmonare.
Un’applicazione innovativa dell’EIT è la sua capacità di valutare la perfusione polmonare utilizzando l’analisi cinetica di un’iniezione di soluzione ipertonica durante un’apnea. La soluzione genera una variazione di impedenza nel torace mentre circola attraverso il sistema vascolare polmonare. Questo metodo indiretto consente di stimare i modelli di perfusione, contribuendo in modo significativo alla nostra comprensione della dinamica del flusso sanguigno polmonare al letto del paziente.
L’EIT non è solo uno strumento per il monitoraggio, ma può anche essere fondamentale per la diagnosi di patologie respiratorie come lo pneumotorace e l’intubazione bronchiale. Può aiutare a identificare l’eziologia della mancata corrispondenza ventilazione/perfusione (V/Q) nei pazienti sottoposti a ventilazione meccanica invasiva, cosa che non è possibile con altri strumenti diagnostici. Inoltre, l’EIT può aiutare nell’ottimizzazione individuale delle impostazioni del ventilatore, come la titolazione della pressione positiva di fine espirazione (PEEP) e il volume corrente che migliorano l’ossigenazione e la salute dei polmoni in terapia intensiva.
In sintesi, l’EIT rappresenta un cambiamento di paradigma nel monitoraggio e nella diagnostica polmonare al letto del paziente. La sua natura non invasiva e l’immediatezza dei dati rendono l’EIT uno strumento indispensabile nella moderna medicina respiratoria. Con le sue crescenti applicazioni, l’EIT sarà fondamentale per far progredire la nostra comprensione e il nostro approccio all’assistenza respiratoria, in particolare in contesti di terapia intensiva.
Introduction
La tomografia ad impedenza elettrica (EIT) è una tecnica di monitoraggio polmonare che traduce le variazioni di impedenza nel tempo in immagini topografiche. Ciò si ottiene iniettando una bassa corrente elettrica alternata (5-10 mA) da elettrodi posizionati circonferenzialmente lungo il tronco (Figura 1A). L’impedenza riflette l’opposizione di un tessuto al flusso di questa corrente elettrica. Durante l’inspirazione, l’impedenza aumenta, mentre diminuisce durante l’espirazione. Un cambiamento simile nell’impedenza si verifica in presenza di fluidi per via endovenosa. Ad esempio, quando i fluidi che hanno una conduttività elettrica più elevata rispetto al sangue vengono iniettati attraverso un catetere centrale, si verifica una corrispondente diminuzione dell’impedenza elettrica 1,2,3,4.
Per praticità, gli elettrodi EIT (in numero di 16 o 32) sono posizionati su una cintura, che viene poi posizionata attorno al torace del paziente, in particolare tra il 4° e il 5°spazio intercostale . Questo posizionamento fornisce una visione ottimale dei polmoni e riduce l’interferenza del diaframma. Nel processo di misurazione, due elettrodi diversi iniettano una corrente preimpostata in sequenza, mentre gli elettrodi rimanenti fungono da ricevitori per le letture di tensione corrispondenti. Questo processo si ripete rapidamente per ogni coppia di elettrodi, ruotando attorno al torace a una frequenza di 20-50 Hz. Questa rapida rotazione è il motivo per cui EIT ha un’alta risoluzione temporale. Un dispositivo EIT toracico calcola la distribuzione dell’impedenza elettrica nella sezione trasversale del torace da ogni ciclo di misurazione e converte questi valori in un’immagine bidimensionale. Questa immagine viene poi visualizzata in tempo reale su un monitor dedicato.
L’EIT ha diverse applicazioni cliniche. Sulla base della tecnologia dell’impedenza, è possibile monitorare la distribuzione dell’aria all’interno del torace e la distribuzione della perfusione, soprattutto quando viene somministrato un mezzo di contrasto per creare variazioni nell’impedenza polmonare. Determinare le impostazioni PEEP per i pazienti ventilati meccanicamente è impegnativo ed essenziale per ridurre al minimo le lesioni polmonari. Inoltre, la sua capacità di tracciare i cambiamenti di ventilazione e perfusione nel tempo offre dati inestimabili per il monitoraggio longitudinale del paziente. Questo aspetto è fondamentale in ambienti clinici dinamici in cui le condizioni del paziente possono evolvere rapidamente5.
L’EIT facilita la visualizzazione non solo della meccanica globale ottenuta attraverso il sensore di flusso o i dati dal ventilatore se il dispositivo EIT è collegato al ventilatore, ma fornisce anche informazioni cruciali sulla sovradistensione e sul collasso regionale 6,7,8,9. Le immagini generate forniscono informazioni funzionali sui polmoni, ma non sono destinate alla diagnosi anatomica e non emettono radiazioni. Negli Stati Uniti d’America, il dispositivo EIT ENLIGHT 2100 è attualmente l’unico approvato dalla Food and Drug Administration (FDA) degli Stati Uniti. Altre aziende sono ora in procinto di ottenere l’approvazione della FDA per l’uso dell’EIT nelle popolazioni adulte, bambini e neonati. Per questo documento, abbiamo utilizzato l’hardware (ad esempio, cinture e schermo), la ventilazione e le mappe di perfusione del dispositivo ENLIGHT 2100.
La configurazione del set EIT include tre apparecchiature essenziali, oltre al monitor stesso, che sono una cintura di elettrodi, il sensore di flusso e il cavo di riferimento. La cintura di elettrodi viene utilizzata per ottenere un’immagine tomografica bidimensionale. L’immagine polmonare EIT è costruita in una rappresentazione bidimensionale con risoluzioni variabili, come 32 x 32, 24 x 24 o 16 x 16 pixel, a seconda delle dimensioni del perimetro del torace e delle specifiche del produttore. Le immagini sono generate dalle misurazioni della tensione utilizzando algoritmi di ricostruzione. Il sensore di flusso è progettato per l’uso su un singolo paziente ed è disponibile in due dimensioni: una per adulti e pazienti pediatrici e un’altra per neonati. Il sensore di flusso adulto-pediatrico non è in grado di misurare un volume corrente inferiore a 40 ml, mentre il sensore neonatale può registrare un volume corrente da 0 a 100 ml. Senza il sensore di flusso, l’EIT visualizza solo i dati di impedenza. Una volta che il sensore di flusso è collegato a un paziente, diventa possibile sincronizzare i dati delle forme d’onda di impedenza con i parametri di pressione, flusso e volume. Il cavo di riferimento è riutilizzabile e funge da punto di riferimento per il valore di iniezione della corrente elettrica.
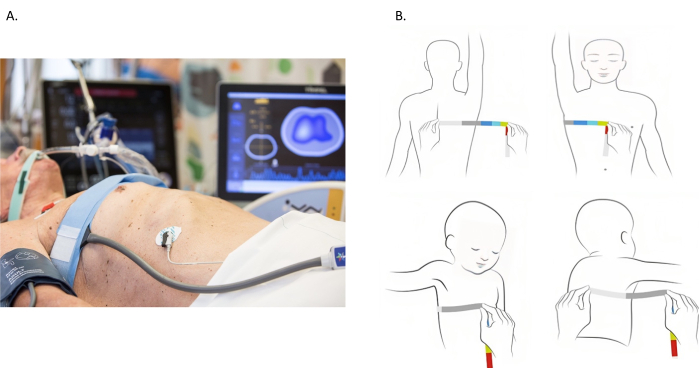
Figura 1: Posizionamento della cintura dell’elettrodo per tomografia ad impedenza elettrica. (A) Cintura di elettrodi per tomografia ad impedenza elettrica posizionata intorno al torace al 4° e 5° spazio intercostale. (B) Misurazione del torace. Il torace viene misurato avvolgendo un metro a nastro attorno a tutto il torace. Tuttavia, la maggior parte dei pazienti è costretta a letto e la misurazione dell’intero torace non è fattibile. Un approccio alternativo è illustrato nelle immagini. Il perimetro del torace viene valutato dal processo spinoso allo sterno. La misurazione viene quindi raddoppiata per tenere conto della parte controlaterale del torace. Clicca qui per visualizzare una versione più grande di questa figura.
L’obiettivo principale di questo documento video è fornire al lettore le conoscenze e le competenze necessarie per diventare esperto nella registrazione e nell’interpretazione delle immagini EIT. Nel perseguimento di questo obiettivo, forniremo una panoramica dei principi dell’EIT, mostreremo le sue capacità di visualizzazione in tempo reale per la distribuzione dell’aria nei polmoni ed esploreremo le sue applicazioni estese nella valutazione della perfusione. Raggiungendo questi obiettivi, miriamo a consentire al pubblico di utilizzare con sicurezza la tecnologia EIT per la valutazione polmonare.
Protocol
Representative Results
Discussion
L’insufficienza respiratoria e la necessità di un intervento di supporto, compresa la ventilazione meccanica invasiva, sono comuni nei pazienti ospedalizzati. Pertanto, il monitoraggio della ventilazione e della perfusione polmonare è fondamentale per una diagnosi e un trattamento tempestivi e personalizzati. A differenza delle tecniche di imaging più standard come i raggi X e la tomografia computerizzata (CT-scan), l’EIT fornisce immagini non invasive e prive di radiazioni dei polmoni e delle loro caratteristiche regionali in tempo reale 1,2,3,4,20. Grazie a queste funzionalità, l’EIT è utile al letto del paziente sia nell’unità di terapia intensiva che in sala operatoria. L’EIT non solo fornisce il monitoraggio della ventilazione, ma offre anche la possibilità di analizzare la perfusione polmonare, cosa che attualmente non è fattibile nella pratica clinica di routine 6,7,8.
Durante la ventilazione meccanica, la protezione del polmone è un obiettivo chiave del trattamento. Uno degli obiettivi è evitare l’atelettasia e l’iperdistensione dei polmoni, che possono portare a lesioni alveolari. Tipicamente, la PEEP viene somministrata per prevenire l’atelettasia e mantenere il volume polmonare. L’identificazione della PEEP ottimale per i singoli pazienti, nota come “titolazione PEEP”, è un metodo cruciale, in particolare in condizioni come la sindrome da distress respiratorio acuto (ARDS), l’obesità e l’ipertensione addominale21,22.
Il metodo convenzionale per la titolazione PEEP si basa sull’ossigenazione e sulla meccanica polmonare. Tuttavia, questo approccio non tiene conto delle alterazioni polmonari regionali e del fatto che le aree del polmone siano iperdistese o collassate. Tecniche avanzate come l’EIT forniscono immagini dettagliate e in tempo reale dei polmoni durante l’inspirazione e l’espirazione. La titolazione PEEP con EIT consente di ottimizzare l’ossigenazione e la meccanica polmonare, riducendo al minimo la sovradistensione e il collasso del parenchima 23,24,25,26,27,28.
Più recentemente, lo strumento di perfusione dell’EIT è stato sviluppato per fornire una valutazione dettagliata del flusso sanguigno polmonare regionale, consentendo ai medici e al personale medico di stimare la relazione ventilazione-perfusione. La perfusione polmonare valutata dall’EIT è stata utilizzata anche per determinare la risposta agli aggiustamenti della ventilazione e all’ossigenazione, nonché la risposta alla terapia vasodilatatrice polmonare 9,23,25,29,30,31. Inoltre, l’EIT può anche rilevare grandi difetti di perfusione polmonare, suggerendo la presenza di tromboembolia32,33.
L’EIT ha alcune controindicazioni. In primo luogo, l’EIT non è attualmente raccomandato nei pazienti con pacemaker o defibrillatori impiantabili. Al momento, non ci sono studi che valutino l’interferenza elettrica del segnale EIT e della funzione del pacemaker. In secondo luogo, il segnale di impedenza può essere alterato da condizioni come pneumomediastino significativo o enfisema sottocutaneo, compromettendo la corretta interpretazione delle mappe di ventilazione e perfusione. Infine, il requisito che la cintura sia a stretto contatto con la pelle presenta sfide nell’uso dell’EIT con pazienti che hanno bende toraciche34.
È fondamentale prestare attenzione ed evitare di utilizzare lo strumento di perfusione in determinati scenari: pazienti che ricevono dosi crescenti di vasopressori; pazienti con ipernatriemia; pazienti con pneumotorace attivo e/o fistola broncopleurica; neonati e pazienti pediatrici. L’utilizzo dell’EIT per la valutazione della perfusione insieme all’imaging della ventilazione tradizionale consente agli operatori sanitari di comprendere più a fondo la funzione polmonare, aiutando nella diagnosi e nel trattamento dei pazienti in vari contesti clinici.
Considerazioni per popolazioni specifiche
I principi della tecnologia EIT si applicano ai neonati, ai pazienti pediatrici e adulti in base al perimetro toracico e alle dimensioni della cintura. Le cinture per neonati sono monouso e consigliano di essere posizionate per 24 ore invece di 48 ore per gli adulti. E’ stato creato uno specifico sensore di flusso in grado di misurare i piccoli volumi correnti (da 3 mL a 100 mL) associati a questa popolazione e aventi un corrispondente spazio morto di 1 mL.
Il monitoraggio online classifica i polmoni in regioni di interesse (ROI) predefinite, ad esempio. quattro metà (sinistra, destra, anteriore e posteriore) o quattro strati orizzontali. Tuttavia, l’analisi offline potrebbe offrire maggiori opportunità per un’analisi approfondita, ad esempio pixel per pixel. Tutti i dati dell’EIT sono conservati in un formato proprietario noto come Product Information Management (PIM). Il file PIM incapsula le informazioni pre-elaborate, tra cui la tensione misurata prima della ricostruzione tomografica, i segnali non filtrati e i parametri di ventilazione. Per estrarre il file PIM per l’analisi offline, collegare un’unità USB allo slot sul dispositivo EIT; Quindi, selezionare il paziente indice. L’analisi offline è utile perché fornisce tutti i dati dettagliati necessari per comprendere la fisiologia polmonare.
Come strumento diagnostico al letto del paziente, l’EIT potrebbe aiutare a diagnosticare condizioni come atelettasia, iperdistensione e pneumotorace. Oltre alla presentazione clinica e all’esame obiettivo, l’EIT offre informazioni dettagliate per queste diagnosi. L’EIT consente un recupero delle informazioni più rapido rispetto all’indagine classica. Questa capacità consente ai medici e ad altro personale sanitario di diagnosticare e trattare prontamente i pazienti 24,35,36,37.
Imparare a utilizzare e interpretare l’EIT è essenziale perché si rivela utile nella pratica clinica. La sua natura non invasiva e le capacità di monitoraggio in tempo reale rendono l’EIT uno strumento prezioso per i medici sanitari in vari contesti medici.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Esprimiamo il nostro sincero apprezzamento a tutti i co-autori per il loro contributo a questo articolo e ringraziamo TIMPEL Medical per aver generosamente supportato questo manoscritto con attrezzature e supporto.
Materials
| EIT equipment (ENLIGHT2100) | Timpel Medical | ||
| Belts | Timpel Medical | ||
| Belt coverage | Timpel Medical | ||
| Flow sensor | Philips | ||
| Reference Cable | Timpel Medical | ||
| Solution with high electrical conductivity (eg. hypertonic saline, sodium bicarbonate) | Not applicable |
References
- Costa, E. L., Lima, R. G., Amato, M. B. Electrical impedance tomography. Curr Opin Crit Care. 15 (1), 18-24 (2009).
- Frerichs, I., et al. Chest electrical impedance tomography examination, data analysis, terminology, clinical use and recommendations: consensus statement of the TRanslational EIT developmeNt stuDy group. Thorax. 72 (1), 83-93 (2017).
- Borges, J. B., et al. Regional lung perfusion estimated by electrical impedance tomography in a piglet model of lung collapse. J Appl Physiol (1985). 112 (1), 225-236 (2012).
- Victorino, J. A., et al. Imbalances in regional lung ventilation: a validation study on electrical impedance tomography. Am J Respir Crit Care Med. 169 (7), 791-800 (2004).
- Heines, S. J. H., et al. Pulmonary pathophysiology development of COVID-19 assessed by serial Electrical Impedance Tomography in the MaastrICCht cohort. Sci Rep. 12 (1), 14517 (2022).
- Nascimento, M. S., et al. Effect of general anesthesia and controlled mechanical ventilation on pulmonary ventilation distribution assessed by electrical impedance tomography in healthy children. PLoS One. 18 (3), e0283039 (2023).
- Zhao, Z., Fu, F., Frerichs, I. Thoracic electrical impedance tomography in Chinese hospitals: a review of clinical research and daily applications. Physiol Meas. 41 (4), 04TR01 (2020).
- Kobylianskii, J., Murray, A., Brace, D., Goligher, E., Fan, E. Electrical impedance tomography in adult patients undergoing mechanical ventilation: A systematic review. J Crit Care. 35, 33-50 (2016).
- Costa, E. L., et al. Bedside estimation of recruitable alveolar collapse and hyperdistension by electrical impedance tomography. Intensive Care Med. 35 (6), 1132-1137 (2009).
- Mendes, P. V., et al. Lung perfusion during veno-venous extracorporeal membrane oxygenation in a model of hypoxemic respiratory failure. Intensive Care Med Exp. 10 (1), 15 (2022).
- Gaulton, T. G., et al. Regional lung perfusion using different indicators in electrical impedance tomography. J Appl Physiol (1985). 135 (3), 500-507 (2023).
- Martin, K. T., et al. Electrical impedance tomography identifies evolution of regional perfusion in a porcine model of acute respiratory dstress syndrome. Anesthesiology. 139 (6), 815-826 (2023).
- Xin, Y., et al. Improving pulmonary perfusion assessment by dynamic contrast-enhanced computed tomography in an experimental lung injury model. J Appl Physiol (1985). 134 (6), 1496-1507 (2023).
- van der Burg, P. S., Miedema, M., de Jongh, F. H., van Kaam, A. H. Unilateral atelectasis in a preterm infant monitored with electrical impedance tomography: a case report. Eur J Pediatr. 173 (12), 1715-1717 (2014).
- Riva, T., et al. Evaluation of atelectasis using electrical impedance tomography during procedural deep sedation for MRI in small children: A prospective observational trial. J Clin Anesth. 77, 110626 (2022).
- He, H., et al. Influence of overdistension/recruitment induced by high positive end-expiratory pressure on ventilation-perfusion matching assessed by electrical impedance tomography with saline bolus. Crit Care. 24 (1), 586 (2020).
- Girrbach, F., et al. Detection of posttraumatic pneumothorax using electrical impedance tomography-An observer-blinded study in pigs with blunt chest trauma. PLoS One. 15 (1), e0227518 (2020).
- Yang, Y., et al. Bedside electrical impedance tomography in early diagnosis of pneumothorax in mechanically ventilated ICU patients – a single-center retrospective cohort study. J Clin Monit Comput. 37 (2), 629-637 (2023).
- Kallio, M., et al. Electrical impedance tomography reveals pathophysiology of neonatal pneumothorax during NAVA. Clin Case Rep. 8 (8), 1574-1578 (2020).
- Pereira, S. M., et al. Individual positive end-expiratory pressure settings optimize intraoperative mechanical ventilation and reduce postoperative atelectasis. Anesthesiology. 129 (6), 1070-1081 (2018).
- Jimenez, J. V., Weirauch, A. J., Culter, C. A., Choi, P. J., Hyzy, R. C. Electrical impedance tomography in acute respiratory distress syndrome management. Crit Care Med. 50 (8), 1210-1223 (2022).
- Becher, T., et al. Individualization of PEEP and tidal volume in ARDS patients with electrical impedance tomography: a pilot feasibility study. Ann Intensive Care. 11 (1), 89 (2021).
- Barbas, C. S. V., Amato, M. B. P. Electrical impedance tomography to titrate PEEP at bedside in ARDS. Respir Care. 67 (8), 1061-1063 (2022).
- Maciejewski, D., Putowski, Z., Czok, M., Krzych, L. J. Electrical impedance tomography as a tool for monitoring mechanical ventilation. An introduction to the technique. Adv Med Sci. 66 (2), 388-395 (2021).
- Jonkman, A. H., et al. Lung recruitment assessed by electrical impedance tomography (RECRUIT): A multicenter study of COVID-19 acute respiratory distress syndrome. Am J Respir Crit Care Med. 208 (1), 25-38 (2023).
- Jimenez, J. V., et al. Electric impedance tomography-guided PEEP titration reduces mechanical power in ARDS: a randomized crossover pilot trial. Crit Care. 27 (1), 21 (2023).
- Sella, N., et al. Electrical impedance tomography: A compass for the safe route to optimal PEEP. Respir Med. 187, 106555 (2021).
- Slobod, D., et al. Integrating electrical impedance tomography and transpulmonary pressure monitoring to personalize PEEP in hypoxemic patients undergoing pressure support ventilation. Crit Care. 26 (1), 314 (2022).
- Spina, S., et al. Modulation of pulmonary blood flow in patients with acute respiratory failure. Nitric Oxide. 136-137, 1-7 (2023).
- Cenci, S., Santiago, R. S., Bittner, E. A., Berra, L. Assessing regional lung perfusion changes to inhaled pulmonary vasodilators by electrical impedance tomography. Am J Respir Crit Care Med. 208 (9), e39-e40 (2023).
- Ekkapat, G., Ribeiro De Santis Santiago, R., Victor, M., Berra, L. Electrical impedance tomography for assessing the impact of inhaled nitric oxide on pulmonary artery pressure. Anesthesiology. , (2024).
- He, H., et al. Bedside evaluation of pulmonary embolism by saline contrast electrical impedance tomography method: A prospective observational study. Am J Respir Crit Care Med. 202 (10), 1464-1468 (2020).
- He, H., et al. Three broad classifications of acute respiratory failure etiologies based on regional ventilation and perfusion by electrical impedance tomography: a hypothesis-generating study. Ann Intensive Care. 11 (1), 134 (2021).
- Ribeiro De Santis Santiago, R., et al. Lung imaging acquisition with electrical impedance tomography: Tackling common pitfalls. Anesthesiology. 139 (3), 329-341 (2023).
- Zhou, R., et al. Electrical impedance tomography to aid in the identification of hypoxemia etiology: Massive atelectasis or pneumothorax? A case report. Front Med (Lausanne). 970087, (2022).
- Rubin, J., Berra, L. Electrical impedance tomography in the adult intensive care unit: clinical applications and future directions. Curr Opin Crit Care. 28 (3), 292-301 (2022).
- Tomicic, V., Cornejo, R. Lung monitoring with electrical impedance tomography: technical considerations and clinical applications. J Thorac Dis. 11 (7), 3122-3135 (2019).

.
