7.9:
원자의 양자역학 모델
7.9:
원자의 양자역학 모델
드 브로글리가 수소 원자의 전자가 정량화된 원형 궤도에서 움직이는 입자 대신 원형 서파로 생각할 수 있다는 자신의 아이디어를 발표한 직후, 에르빈 슈뢰딩거는 현재 슈뢰딩거 방정식으로 알려진 것을 도출하여 드 브로글리의 작품을 확장했다. 슈뢰딩거가 수소와 같은 원자에 자신의 방정식을 적용했을 때, 그는 에너지에 대한 보어의 표현을 재현할 수 있었고, 따라서 수소 스펙트럼을 지배하는 Rydberg 공식을 재현할 수 있었습니다. Schrödinger는 전자를 그리스 문자 psi로 표현되는 3차원 고정 파동 또는 파기능으로 묘사했으며, ψ.
몇 년 후, 맥스 태어난 여전히 오늘날 허용되는 파장 ψ 해석을 제안 : 전자는 여전히 입자이며, 그래서 ψ 표현 파도는 물리적 파도가 아니라, 대신, 복잡한 확률 진폭이다. 파기능 의 크기의 사각형 â£ψâ£2 공간의 특정 위치 근처에 존재하는 양자 입자의 확률을 설명합니다. 이는 파동 기능을 사용하여 원자에서 핵에 대하여 전자밀도의 분포를 결정할 수 있다. 가장 일반적인 형태로 Schrödinger 방정식은 다음과 같이 작성할 수 있습니다.
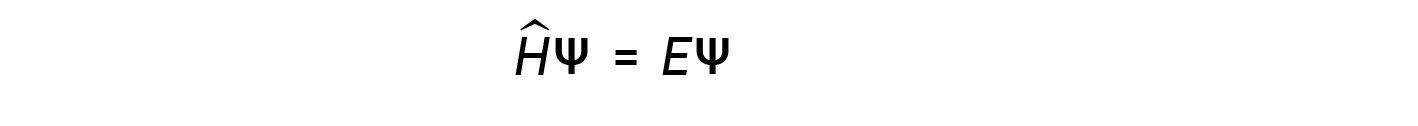
여기서, Ĥgt; 해밀턴 연산자, 양자 입자의 총 에너지 (전위 플러스 운동)를 나타내는 일련의 수학 작업 (예: 원자내 전자), ψ 입자를 찾는 확률의 특별한 분포를 찾아 내기 위해 사용될 수 있는 이 입자의 파동기능이며, E는 입자의 총 에너지의 실제 값이다.
슈뢰딩거의 작품뿐만 아니라 하이젠베르크와 다른 많은 과학자들이 그들의 발자취를 따르는 작품은 일반적으로 양자 역학이라고 합니다.
양자 기계 모델은 전자를 찾을 확률이 가장 높은 원자 내의 핵 주위의 3차원 공간으로 궤도를 설명합니다.
