16.2:
缓冲液
このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
JoVE Core
化学
Buffers
向溶液中加入少量的酸或碱,可导致 pH 值显著降低或升高。然而,许多化学和生物化学过程 需要一个稳定的 pH 值才能发挥作用。缓冲液可以防止溶液的 pH 值发生剧烈变化,在没有超过它们缓冲能力的情况下。缓冲液含有弱酸及其共轭碱 或弱碱及其共轭酸。例如,人类血液将其 pH 值保持在 7.4 附近,通过一种缓冲液,由碳酸(一种弱酸)和碳酸氢根离子(它的共轭碱)组成。共轭酸碱对会形成缓冲液,是因为它们不会中和它们的共轭酸或碱。例如,醋酸和醋酸盐不能反应。然而,如果把醋酸(一种弱酸)和氨(一种弱碱)加在一起,它们就会反应生成一种盐—醋酸铵。在缓冲液中,弱酸通过与产生的氢氧化物离子 反应来中和任何添加的碱,而其共轭碱通过与任何水合氢离子 反应来中和任何添加的酸。类似的机制也适用于弱碱 及其共轭酸的情况下。两个烧杯,X 和 Y,含有相同体积的 不同溶液,每个溶液的 pH 值为 7.2。烧杯 X 中的溶液没有进行缓冲。相反,烧杯 Y 中的溶液 含有乙酸-醋酸盐缓冲液。如果向烧杯 X 中添加盐酸,溶液的 pH 值会由于 水合氢离子浓度的增加 而突然下降。相反,烧杯 Y 中的溶液 烧杯 Y 中的溶液显示出几乎恒定的 pH 值,因为其中一种缓冲组分,醋酸盐,与盐酸反应,生成 氯离子和醋酸。同样地,如果向烧杯 X 中添加氢氧化钠,溶液的 pH 值会由于 氢氧化物离子浓度的增加 而突然升高。另一方面,当向烧杯 Y 中添加 氢氧化钠时,烧杯 Y 中的溶液的 pH 值 变化很小,因为其中一种缓冲组分,醋酸,与氢氧化钠反应,生成乙酸钠 和水分子。只要共轭酸碱对在溶液中的浓度高于 加入的强酸或强碱浓度,缓冲液就可以 防止溶液的 pH 值发生剧烈变化。
16.2:
缓冲液
包含大量弱共轭酸碱对的溶液称为缓冲溶液或缓冲液。 添加少量强酸或强碱时,缓冲溶液可抵抗 pH 值的变化。 乙酸和乙酸钠的溶液是由弱酸及其盐组成的缓冲液的一个示例: CH3COOH (AQ) + CH3COONA (AQ)。 由弱碱及其盐组成的缓冲液的一个示例是氨和氯化铵的溶液: NH3 (AQ) + NH4Cl (AQ)。
缓冲液的工作原理
为了说明缓冲溶液的功能,请考虑一种醋酸和乙酸钠含量大致相等的混合物。 溶液中存在弱共轭酸碱对,这削弱了抵消少量新增强酸或碱的能力。 例如,在该溶液中添加强碱将中和水合氢离子,并将乙酸电离平衡转移到右侧,从而部分恢复降低的 H3O+ 浓度:
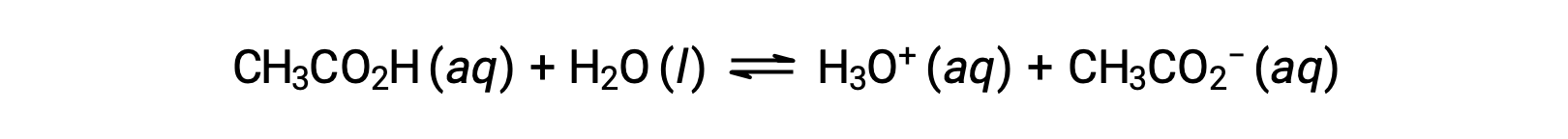
同样,向该缓冲溶液添加强酸将中和乙酸酯离子,使上述电离平衡向右移动,并使 [H3O+] 恢复到接近其原始值。 图 1 提供了添加强酸和碱时对缓冲溶液所做更改的图形说明。 溶液的缓冲操作基本上是由添加的强酸和碱转换为组成缓冲区共轭对的弱酸和碱引起的。 与强酸和碱的完全电离相比,弱酸和碱只会发生轻微电离。 因此,溶液 pH 值的变化远低于无缓冲溶液中的变化。

图 1. 乙酸和醋酸盐混合物中的缓冲作用。
本文改编自 Openstax, 化学 2e, 第14.6节:缓冲液。
