16.1:
同离子效应
このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
JoVE Core
化学
Common Ion Effect
醋酸,一种弱酸,在溶液中 部分解离产生水合氢离子和醋酸盐 离子,而它的盐,乙酸钠,则完全解离产生钠离子 和醋酸盐。醋酸和乙酸钠 都有共同的醋酸盐离子。当在醋酸溶液中加入乙酸钠时,它增加了醋酸根离子的总浓度,扰乱了平衡。为了抵消这种变化,平衡 向左侧移动并导致醋酸的产生,直到平衡被重新建立。在这种情况下,共同离子的存在 导致了化合物的解离减少。这种现象被称为共同离子效应。共同离子效应可以在 勒沙特列原理的帮助下来解释,该原理 指出,平衡时反应物或产物浓度的 变化将导致体系向 抵消这种变化的方向移动。0.050M 氨溶液的 pH 值为 10.97。如果在溶液中加入 0.040M 的氯化铵,新的 pH 值可以用氨的碱离解 常数和 ICE 表来确定。氯化铵完全电离产生 0.040M 的 铵离子和氯离子。由于氯离子是 pH 中性的,所以可以忽略它们。氨部分分解产生铵离子和氢氧化物 离子。该反应的 Kb 为 1.76×10⁻⁵,等于铵离子的浓度乘以 氢氧化物离子的浓度除以 氨的浓度。初始浓度、变化浓度和平衡 浓度的值放在 ICE 表中,浓度的变化用 x 表示。由于 x 的值很小,0.050 减去 x 大约 等于 0.050,0.040 加上 x 大约 等于 0.040,这可以稍后用 5%规则进行验证。将这些值代入 Kb 的表达式中,x 等于 2.2×10⁻⁵M。因为氢氧化物浓度小于 0.040 M 的 5%该近似是有效的。溶液的 pOH 和 pH 值可以 使用标准方程式来计算,分别等于 4.66 和 9.34。因此,共同离子,铵离子的存在,导致氨的离解减少,从而将溶液的 pH 值 从 10.97 降低到 9.34。
16.1:
同离子效应
与纯水相比,含有普通离子的水溶液 (离子化合物的溶解也产生的离子) 离子化合物的溶解度较低。 这是一个称为同离子效应的现象的示例,这是质量作用定律的结果,可以使用 勒夏特列原理(Le Chatelier’s Principle) 来解释。 考虑碘化银的溶解:
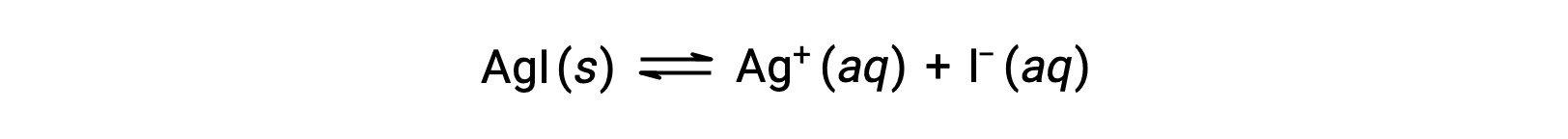
这种溶解平衡可能会因添加银 (I) 或碘化离子而改变,从而导致 AGI 的沉淀和溶解 AA+ 和 I –的浓度降低。 在已经含有这两种离子之一的溶液中,没有这些离子的 AGI 可能比溶液中的溶解更少。
这种影响也可以用溶度积表达式中表示的质量操作来解释:
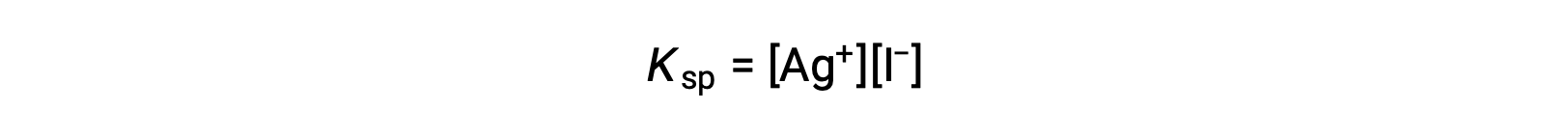
无论离子源如何,银 (i) 和碘化离子极性的数学生成物在平衡混合物中都是恒定的,因此一个离子的浓度的增加必须通过另一个离子的比例减小来平衡。
关于溶解度的同离子效应
常见离子会影响化合物在溶液中的溶解度。 例如,固体 mg/OH)2 解离 Mg2+ 和 OH− 离子,如下所示;
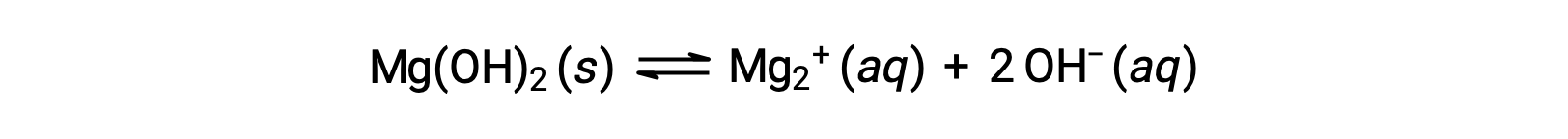
如果将 MgCl2 添加到饱和溶液 (mg/Oh) 2 中,则反应将向左移,以根据 Le Châtelier 的原理释放附加 Mg2+ 离子产生的应力。 在定量的术语中,添加的 Mg2+ 会导致反应商大于溶度积 (Q > KSP) ,而 MG (OH) 2 表单会一直到反应商再次等于 KSP 为止。 在新的平衡状态下, [mg-] OH 小于 [Mg2+] ,且 [Mg2+] 大于纯水中的 mg/OH)2 溶液。
如果 Koh 被添加到饱和溶液 (毫克 (OH) 2 中,反应将向左移以释放额外 OH 离子的应力。 MG (OH) 2 形成,直到反应商再次等于 KSP。 在新的平衡状态下, [mg-2+] OH 大于 [Mg2+] ,小于纯水中的 mg/OH)2 的溶液。
