16.4:
计算缓冲溶液中的 pH 值变化
Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
JoVE Core
Chimie
Calculating pH Changes in a Buffer Solution
当加入少量的强酸或 加入少量的强碱时,缓冲溶液中会出现轻微的 pH 值变化。这个 pH 值变化是分两个不同的步骤计算出来的。首先,使用化学计量计算 来确定浓度的变化。然后,通过平衡计算 确定溶液的新 pH 值,可以使用 ICE 表,或者亨德森-哈塞尔巴尔赫方程。含有 2.0M 氢氟酸和氟化钠的 缓冲液的 pH 值 可以在加入强酸或强碱之前和之后 进行计算。亨德森-哈塞尔巴尔赫方程 可用于确定该缓冲液的初始 pH 值,因为该浓度相对于 弱酸的 Ka 较高,且浓度的变化 小于 5%氢氟酸的 pKa 值可计算为 3.46。当溶液中弱酸和共轭碱的 浓度相等时,pH 值等于 pKa 值。因此,初始 pH 值为 3.46。如果将 0.2 摩尔的盐酸 添加到一升缓冲液中,假设其引起的体积变化 可以忽略不计,则添加的酸 被氟离子中和,产生氢氟酸。这导致氟离子浓度的 化学计量比降低 0.2 摩尔,而氢氟酸浓度 也有相同的增加。新的浓度可以插入 亨德森-哈塞尔巴尔赫方程。求解后,新的 pH 值为 3.37,小于初始的 pH 值 3.46。当加入强酸时,pH 值会降低,但由于溶液是被缓冲的,所以 降低的幅度很小。相反,如果将 0.1 摩尔的氢氧化钠 添加到一升缓冲液中,假设其引起的体积变化 可以忽略不计,则加入的碱 通过与氢氟酸反应而被中和。这导致氢氟酸浓度的 化学计量比降低 0.1 摩尔,而氟离子的化学计量同等增加。使用 Henderson-Hasselbalch 方程,溶液的 pH 值为 3.50,由于 添加了氢氧化钠,该值略高于 初始 pH 值 3.46。
16.4:
计算缓冲溶液中的 pH 值变化
缓冲液可以防止在将强酸或碱增加到缓冲容量后溶液的 pH 值突然下降或升高;但是,这种增加强酸或碱确实会导致溶液的 pH 值轻微变化。 小 pH 值变化可通过确定计算得出缓冲液成分浓度的变化,即弱酸及其共轭碱,反之亦然。 使用这些化学化学当量计算得出的浓度可用于使用 亨德森-哈塞尔巴尔赫方程(Henderson-Hasselbalch Equation) 或 ICE表格 确定溶液的最终 pH 值。
例如,缓冲溶液含有 0.65 mol 的甲酸和钠甲酸。 由于弱酸的浓度及其共轭碱在这里是相同的,溶液的 pH 值等于弱酸的 pKa ,在本例中为 3.74。 如果将 0.05 mol HNO3 添加到该溶液中,则可通过化学化学计量计算来确定形成酸和形成钠的浓度的结果变化,如下表所示。
| H+ (AQ) | HCOO− (AQ) | HCOOH (AQ) | |
| 添加前 (M) | ~0.00 摩尔 | 0.65 摩尔 | 0.65 摩尔 |
| 新增 (M) | 0.050 摩尔 | -- | |
| 添加后 (M) | ~0.00 摩尔 | 0.60 摩尔 | 0.70 摩尔 |
然后,可以通过将改变的甲酸和甲酸钠浓度插入 亨德森-哈塞尔巴尔赫方程(Henderson-Hasselbalch Equation) 来确定溶液的最终 pH 值。
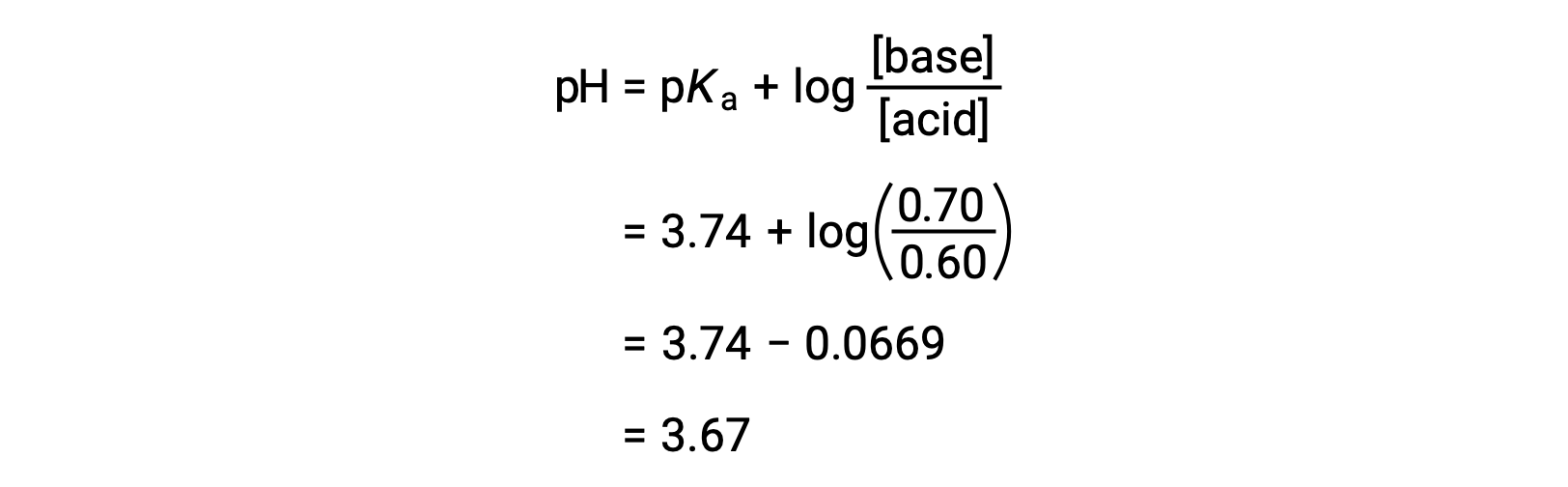
因此,增加 0.05 摩尔的 HNO3 可将溶液的 pH 值从 3.74 降至 3.67。
同样,如果将 0.10 mol NaOH 添加到同一个溶液中,则可通过化学计量计算来确定形成酸和形成钠的浓度的结果变化,如下表所示。
| OH− (AQ) | HCOOH (AQ) | HCOO− (AQ) | 水 (升) | |
| 添加前 (M) | ~0.00 摩尔 | 0.65 摩尔 | 0.65 摩尔 | - |
| 新增 (M) | 0.10 摩尔 | -- | | |
| 添加后 (M) | ~0.00 摩尔 | 0.55 摩尔 | 0.75 摩尔 | |
然后,可以通过将改变的甲酸和甲酸钠浓度插入 亨德森-哈塞尔巴尔赫方程(Henderson-Hasselbalch Equation) 来确定溶液的最终 pH 值。
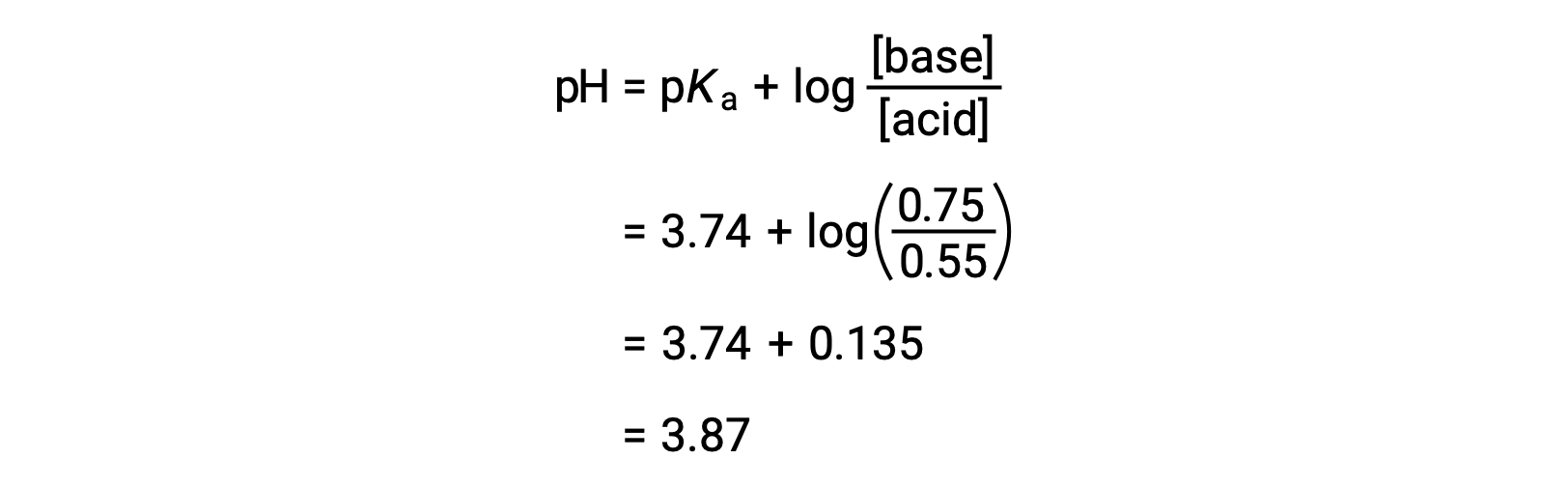
因此,添加 0.10 mol NaOH 后,溶液的 pH 值从 3.74 增加到 3.87。
