Structurele Informatie van Single-molecule FRET experimenten met de Fast Nano-positioneringssysteem
Summary
We present the setup and experimental procedure to obtain smFRET data from large donor-acceptor networks with a TIRF microscope. The step-by-step analysis of these measurements with the Bayesian inference software Fast-NPS yields high-resolved structural information via the application of adapted dye models.
Abstract
Single-molecule Förster Resonance Energy Transfer (smFRET) can be used to obtain structural information on biomolecular complexes in real-time. Thereby, multiple smFRET measurements are used to localize an unknown dye position inside a protein complex by means of trilateration. In order to obtain quantitative information, the Nano-Positioning System (NPS) uses probabilistic data analysis to combine structural information from X-ray crystallography with single-molecule fluorescence data to calculate not only the most probable position but the complete three-dimensional probability distribution, termed posterior, which indicates the experimental uncertainty. The concept was generalized for the analysis of smFRET networks containing numerous dye molecules. The latest version of NPS, Fast-NPS, features a new algorithm using Bayesian parameter estimation based on Markov Chain Monte Carlo sampling and parallel tempering that allows for the analysis of large smFRET networks in a comparably short time. Moreover, Fast-NPS allows the calculation of the posterior by choosing one of five different models for each dye, that account for the different spatial and orientational behavior exhibited by the dye molecules due to their local environment.
Here we present a detailed protocol for obtaining smFRET data and applying the Fast-NPS. We provide detailed instructions for the acquisition of the three input parameters of Fast-NPS: the smFRET values, as well as the quantum yield and anisotropy of the dye molecules. Recently, the NPS has been used to elucidate the architecture of an archaeal open promotor complex. This data is used to demonstrate the influence of the five different dye models on the posterior distribution.
Introduction
Het bepalen van de structuur van een biomolecuul is een belangrijke voorwaarde voor het begrijpen van zijn functie. Twee goed gevestigde methoden voor structuurbepaling zijn cryo-elektronenmicroscopie en X-ray kristallografie 1, 2. Vandaag, beide methoden bieden een hoge-resolutie structurele informatie met een resolutie tot aan de Angstrom niveau. Deze twee methoden zijn uitgebreid gebruikt om de structuur van grote biomoleculen zoals helderen eiwitcomplexen. Hoewel de bestaande werkwijzen continu gedurende de laatste jaren verbeterd, de complexiteit van biologische structuren vormt nog steeds een belangrijke uitdaging voor structurele biologie, in het bijzonder bij grote, dynamische en kortlevende complexen onderzocht 3.
Om de dynamiek van macromoleculaire complexen en de structuur-functie relatie name bestuderen single-molecule methodologieën provided nuttige informatie 4. Verschillende nieuwe strategieën ontwikkeld verschaffen van een orthogonale aanpak op het verwerven van structurele en dynamische informatie. Voorbeelden zijn hoge snelheid AFM 5, mechanische manipulatie 6, fluorescentie microscopie lokalisatie 7, evenals individuele molecuul Förster Resonance Energy Transfer (smFRET) 8, 9. Aangezien al vroeg FRET is genoemd moleculair liniaal, door de afstand afhankelijkheid van de lengteschaal van biomacromoleculen 10.
Een bijzonder interessante toepassing van smFRET is de afstand informatie van smFRET metingen gebruiken om afleiden structurele informatie 11, 12, 13, 14, 15 </sup>, 16, 17, 18, 19, 20, 21, 22, 23. Vanwege de hoge tijdsresolutie van smFRET kan de positie van de beweegbare delen van een eiwitstructuur worden gelokaliseerd. Echter, om kwantitatieve informatie smFRET data belangrijk correctieparameters de kleurstofmoleculen extraheren moet tijdens de meting 24 te bepalen. Met deze correctiefactoren, kan de FRET efficiëntie E FRET worden berekend met de formule
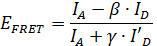 ,
,
waar ik A pt I D </sub> de fluorescentie-intensiteit van de donor en de acceptor molecule zijn (zie figuur 2). De β-factor is goed voor cross-talk, het lekken van donor-emissie in de acceptor kanaal en wordt berekend door

waarin I 'en A Ik zou de fluorescentie-intensiteit van de donor en de acceptor molecule na bleken door het acceptormolecuul.
Het γ-factor corrigeert het verschil in de relatieve detectie-efficiëntie van de twee kanalen en de verschillen in de fluorescentie kwantumopbrengst van de donor en de acceptor kleurstof. Het wordt berekend op basis van elk individu tijd spoor door
<p class="jove_content" fo:keep-together.within-page="1" fo:text-align="center" style = "text-align: center;">
Merk op, dat deze beschrijving verwaarloost directe excitatie van de acceptor molecule, die soms belangrijk wordt en zou moeten worden gecorrigeerd ook. Voor het vaststellen van deze correctiefactoren is het nuttig om zowel de donor als de acceptor wekken in een afwisselend schema 25 om onderscheid te maken tussen foto-fysische veranderingen en structuurdynamica.
Om niet alleen kwantitatieve smFRET efficiëntie maar ook kwantitatieve structurele informatie te verkrijgen, de Nano-Positioning System (NPS) werd in 2008 26. De naam werd gekozen op basis van de overeenkomsten met de satelliet-gebaseerde Global Positioning System (GPS). De NPS is een hybride techniek combineert smFRET en röntgenkristallografie gegevens voor het lokaliseren van onbekende kleurstof posities in Biomacromoleculaire complexen. de crystal structuur fungeert als referentieframe en de smFRET resultaten worden gebruikt om informatie afstand tussen een onbekende fluorofoor positie (antenne) en staat bekend uit de kristalstructuur (satelliet) te verkrijgen. In opeenvolgende experimenten werd de afstand tussen de antenne en meerdere satellieten worden gemeten en de positie van de antenne wordt bepaald met behulp van een statistisch rigoureuze analyseschema Bayesian parameterschatting. Daardoor is niet alleen de meest waarschijnlijke positie van de antenne berekend, maar de volledige 3D onzekerheid distributie, de zogenaamde posterior, gevisualiseerd door geloofwaardige volumes. Bovendien NPS uitgebreid, teneinde de analyse van complete netwerken smFRET 27.
De NPS is gebruikt om een aantal belangrijke vragen in eukaryote transcriptie, namelijk tijdens het stroomopwaartse DNA, de niet-matrijs-DNA en de ontluikende mRNA in het RNA polymerase II elongatie co lossenmplex 12, 28, blijkt ook het effect van transcriptie initiatie factoren 26 en de dynamische architectuur van een open-promotor complex 29. Bovendien, de NPS werd gebruikt om de structuur van de Archaea RNA Polymerase geopend complex 30 met name de positie van transcriptie initiatie factor TFE, die competitief aan dezelfde plaats als transcriptiefactor elongatie factor Spt4 / 5 31 helderen.
Sindsdien zijn er een aantal smFRET gebaseerd structurele aanpak is gepubliceerd op 15, 18, 21, 23. Bij het vergelijken van verschillende smFRET gebaseerd structurele methoden, wordt duidelijk dat de schijnbare nauwkeurigheid van de werkwijze sterk afhankelijk van de bepaalde keuze van kleurstof modellen. Men moet er rekening mee datkleurstofmoleculen kunnen verschillende ruimtelijke en oriënterende gedrag vertonen afhankelijk van de lokale omgeving.
Hiertoe werd Fast-NPS 32 geïntroduceerd. Fast-NPS maakt gebruik van een geavanceerde sampling algoritme het verminderen van de rekentijden drastisch. Bovendien, Fast-NPS maakt het mogelijk om een structurele analyse uit te voeren en voor elke kleurstof molecule kan de gebruiker kiezen uit een reeks van vijf verschillende kleurstof modellen die volgende zal worden beschreven. De meest conservatieve model, de zogenaamde klassieke, gaat ervan uit dat de kleurstof neemt slechts één, maar onbekende, positie. Bij deze stand kan de fluorofoor vrij draaien binnen een kegel, waarvan de grootte wordt bepaald door zijn respectieve (tijdsafhankelijke) fluorescentie anisotropie. De oriëntatie van de conus is onbekend, wat leidt tot grote onzekerheden bij het converteren van gemeten smFRET efficiëntie in afstanden. In dit opzicht is het model conservatief, omdat het leidt tot de kleinste precisie vergeleken met andere kleurstoffen modusls. Alleen voor zeer korte afstanden moet de aannames van het klassieke model leiden tot een merkbaar onjuiste positiebepaling. Voor typische smFRET waarden wordt de juiste positie steeds ingesloten in het relatief grote volume geloofwaardig.
Aangezien een hogere nauwkeurigheid gewenst is, is het belangrijk om te ontwikkelen en te testen alternatieve modellen kleurstof, die kan bijdragen tot de nauwkeurigheid te verbeteren. Als de kleurstof veel sneller dan zijn inherente fluorescentie levensduur roteert, kan de zogenaamde iso model worden toegepast. Hier is de oriëntatie factor K2 (nodig voor het berekenen van de karakteristieke isotrope Förster radius  ) Is ingesteld op 2/3. Dientengevolge, de berekende geloofwaardige volumes bijna twee orden van grootte kleiner in vergelijking met die in de klassieke model 32. In het geval dat de fluorofoor in een omgeving die niet alleen snel maakt reorientatie, maar daarnaast snelle beweging over haar toegankelijke volume moet de meanpos-iso-model worden gebruikt. In dit model, de kleurstof effectief neemt slechts een gemiddelde positie, waarbij de ruimtelijke middeling wordt verklaard door een polynoom afstand conversie 15. Dit model is van toepassing als bijvoorbeeld de (algemeen hydrofobe) kleurstof wordt een hydrofiel gebied, bijvoorbeeld het DNA bevestigd. Toepassing van de meanpos iso-model leidt tot een verdere verkleining van de geloofwaardige volumes met een factor van ongeveer twee. Echter, kan een kleurstof gebonden aan een eiwit reversibel binden aan verscheidene hydrofobe vlekken in het sterisch toegankelijke volume (AV). Een fluorofoor dat onmiddellijk schakelt tussen deze regio's, maar binnen één regio ondergaat vrije rotatie en snelle gelokaliseerde beweging wordt het best beschreven door de var-meanpos-iso-model. Voor een vergelijkbare situatie waarbij de kleurstof niet vrij de var-meanpos model geldt roteren. meer d IJZE over deze modellen kunt u vinden in onze recente publicatie 32.
) Is ingesteld op 2/3. Dientengevolge, de berekende geloofwaardige volumes bijna twee orden van grootte kleiner in vergelijking met die in de klassieke model 32. In het geval dat de fluorofoor in een omgeving die niet alleen snel maakt reorientatie, maar daarnaast snelle beweging over haar toegankelijke volume moet de meanpos-iso-model worden gebruikt. In dit model, de kleurstof effectief neemt slechts een gemiddelde positie, waarbij de ruimtelijke middeling wordt verklaard door een polynoom afstand conversie 15. Dit model is van toepassing als bijvoorbeeld de (algemeen hydrofobe) kleurstof wordt een hydrofiel gebied, bijvoorbeeld het DNA bevestigd. Toepassing van de meanpos iso-model leidt tot een verdere verkleining van de geloofwaardige volumes met een factor van ongeveer twee. Echter, kan een kleurstof gebonden aan een eiwit reversibel binden aan verscheidene hydrofobe vlekken in het sterisch toegankelijke volume (AV). Een fluorofoor dat onmiddellijk schakelt tussen deze regio's, maar binnen één regio ondergaat vrije rotatie en snelle gelokaliseerde beweging wordt het best beschreven door de var-meanpos-iso-model. Voor een vergelijkbare situatie waarbij de kleurstof niet vrij de var-meanpos model geldt roteren. meer d IJZE over deze modellen kunt u vinden in onze recente publicatie 32.
Deze modellen bieden een uitgebreid repertoire om specifiek rekening te houden met de verschillende omgevingen een kleurstof tegenkomen en de toepassing ervan optimaliseert wijselijk de lokalisatie precisie. Fast-NPS elke kleurstof molecuul gekoppeld aan een bepaalde positie kan worden toegewezen aan een specifiek voertuig, zodat FRET-partners mogen verschillende modellen. Dit maakt het mogelijk onbeperkt en close-to-natuur modellering. Het is echter belangrijk dat men voert strikt statistische proeven uit teneinde de door de uiteindelijke modellencombinatie resultaat nog steeds in overeenstemming met de experimentele gegevens. Deze tests zijn in de Fast-NPS software.
Om Fast-NPS toepassing op experimentele gegevens van de meting (alleen) drie invoerparameters vereist. Ten eerste, de kleurstof-pair specifieke isotrope Förster radii (/54782/54782eq5.jpg "/>) Moeten worden bepaald. Daarom is de kwantumopbrengst (QY) van de donorkleurstof, de donor fluorescentie-emissiespectra en de acceptor absorptie spectra te meten nodig. Deze metingen kunnen worden uitgevoerd in bulk, met een standaard spectrometer en een standaard fluorescentie spectrometer. Voor elk paar, het R 0 wordt vervolgens berekend met de freeware PhotochemCAD en kan worden gebruikt in de NPS analyse. Ook de (Tijdsgeresolveerde) fluorescentie anisotropie van de kleurstofmoleculen moeten worden verkregen met een polarisatie (en tijd) gevoelige fluorescentie spectrometer. de belangrijkste invoerparameters voor Fast-NPS zijn smFRET rendementen gemeten op een enkel-molecuul fluorescentie microscopie setup, zoals een totale interne reflectie fluorescentie microscoop (TIRFM) .
Hier presenteren we een stap-voor-stap protocol voor het verkrijgen smFRET databank toepassen Fast-NPS (figuur 1).
Protocol
Representative Results
Discussion
We presenteren de opzet en experimentele procedure nauwkeurig te bepalen FRET efficiënties tussen kleurstoffen verbonden via flexibele linkers aan biomacromoleculen, dwz, nucleïnezuren en / of eiwitten.
Om te garanderen smFRET nauwkeurige metingen (paragraaf 3), is het cruciaal om lucht uit de stromingskamer dat op elk moment tijdens de meting. Bovendien, zorg ervoor dat niet te veel stroom kamer met fluoroforen. De fluoroforen moeten duidelijk gescheiden om een correcte analyse te waarborgen. Zoals smFRET paren, die niet bleken van de donor vertonen hebben van de analyse uitgesloten, ervoor zorgen dat> 80% van de moleculen in het gezichtsveld worden gebleekt op het einde van de film. Om rekening te houden inhomogeniteiten in het monster de β-factor en de γ-factor corrigeren van overspraak en relatieve detectie efficiency van de donor en acceptor kanaal respectievelijk worden voor elk afzonderlijk FRET paar.
<p class= "Jove_content"> De camera-instellingen (integratie tijd, electron multiplier gain, voorversterker gain en uitlezing tarief in paragraaf 3.9 beschreven) moet worden ingesteld op waarden van het geven van de beste afweging tussen de signaal-ruisverhouding, dynamisch bereik en tijdsresolutie. Ze moeten opnieuw worden afgesteld voor verschillende experimenten of andere hardware wordt gebruikt. Het aantal frames moeten hoog genoeg zodat het merendeel van de donor moleculen bleken binnen de observatietijd worden.Voor de metingen van de fluorescentie spectrometer (Secties 7 tot 9) een goed compromis tussen de signaalintensiteit en de spectrale resolutie van de geregistreerde gegevens worden gevonden. Daartoe de sleuven in de excitatie en emissie route van de fluorescentie spectrometer hebben afhankelijk van het gebruikte instrument en het monster concentratie worden aangepast.
Bovendien presenteren we de Fast-NPS analysemethode om structurele informatie van voorbijgaande of dynamische Macrom verkrijgenolecular complexen. NPS is toegepast op het pad van de niet-matrijs-DNA-streng en de positie van transcriptie initiatie factoren in het archeale RNA polymerase geopend complex onthullen. Via het netwerk van meer dan 60 verschillende afstandsmetingen we aangetoond dat Fast-NPS, voorzien van een nieuw geïmplementeerde sampling engine (Dave, T., Beckers, M., Drechsler, F. & Michaelis, J. in voorbereiding), vermindert de tijd die nodig is voor de analyse van dit complex smFRET netwerk ≈2 orden van grootte in vergelijking met de oorspronkelijke globale methode NPS 27. robuustheid van het algoritme is geworteld in een Metropolis-within-Gibbs sampler gecombineerd met een parallel tempering regeling. Fast-NPS toont exacte reproduceerbaarheid van het netwerk van de resultaten en stemt overeen met de resultaten eerder 30 gepubliceerd.
Verschillende methoden zijn gepubliceerd gericht op structurele informatie afleiden uit smFRET metingen 11 </sup>, 12, 13, 14, 15, 16, 17, 18. Al deze benaderingen slechts één specifieke kleurstof model. Aldus kleurstoffen, die de aannames van die modellen voldoen, kan niet worden gebruikt of leiden tot vals structurele informatie. Snel NPS daarentegen, maakt het mogelijk om kiest per kleurstofmolecuul een ander model. Dit helpt om rekening te houden verschillende conformationeel gedrag van zowel de kleurstof molecuul zelf, evenals de linker voor de bevestiging. De lokale omgeving van de moleculaire kleurstofmolecuul, evenals de fysische eigenschappen bepalen welk model het meest geschikt is.
Voor de geanalyseerde smFRET netwerk van de Archaea initiatiecomplex, een isotrope aanname voor kleurstofmoleculen leidt tot een drastische afname in de grootte van de geloofwaardige volumes in vergelijking met het klassieke model. In combinatie met een dynamische functie gemiddeld voor verfmoleculen de mediaan van alle geloofwaardige volume maten (95%) beperkt tot minder dan 0,5 nm 3. Echter, deze kleurstofmolecuul posteriors zijn niet meer met hun smFRET metingen aangeeft dat de veronderstellingen leiden tot vals structurele informatie. In tegenstelling, de in het klassieke model posteriors zijn consistent met de bepaalde smFRET efficiëntie.
Van de hypothese van isotrope en / of dynamische functie gemiddelde voor alle kleurstoffen leiden tot inconsistenties Fast-NPS maakt kleurstofmolecuul prioren waarbij elke kleurstof kan worden toegewezen een van de vijf modellen. Elk model maakt gebruik van dezelfde toegankelijke volume. Het algoritme voor de berekening van de kleurstof AVS maakt aantal aannamen. Eerst wordt de ruimtelijke vorm van de fluorofoor is benaderd door een bol. Dus een diameter inachtneming wid het fluorofoor'sth, hoogte en de dikte moet worden gebruikt (artikel 12). Verder is het verbindingsstuk van vorm benaderd door een flexibele stang. De in artikel 12 waarden werden berekend voor de kleurstof Alexa 647 gekoppeld via een 12-C linker. Tot op heden is het niet mogelijk om nauwkeurig te bepalen a priori welk model het meest geschikt is, aangezien een experimentele geometrie, en dus alle modellen worden getest. In het algemeen zal men het model dat de kleinst mogelijke afmetingen geeft achterste kiezen, terwijl het nog steeds in overeenstemming met de gegevens. Nagaan modelkeuze is met de smFRET data berekenen we zowel het achterste en de waarschijnlijkheid. Consistentie betekent dat meer dan 90% van de vanuit het achterste monsters binnen het 95% betrouwbaarheidsinterval van de waarschijnlijkheid.
Hoewel het waar is dat hoe lager de anisotropie, hoe kleiner de afstand onzekerheid in een netwerk smFRET geometrische opstellingen van de kleurstofmoleculen moeten ook in aanmerking worden genomen. Dus, terwijl representing kleurstofmoleculen met een lage fluorescentie anisotropie met een iso-model is een typische eerste keus, de consistentie test geeft een meer directe manier voor het selecteren van de juiste kleurstof model. De optimale keuze van kleurstof modellen kunnen leiden tot een drastische verhoging lokalisatie precisie en tegelijkertijd behouden consistentie van het netwerk met FRET data.
Om samen te vatten, Fast-NPS maakt het mogelijk om structurele en dynamische informatie van grote macromoleculaire complexen te krijgen. In tegenstelling tot normale structuur werkwijzen zoals x-ray kristallografie of cryo elektronenmicroscopie dit voeren ter controle zeer flexibele of transient complexen, dus sterk verruimen onze mechanistisch begrip van complexe biologische processen.
Declarações
The authors have nothing to disclose.
Acknowledgements
The authors thank B. Gruchmann for the mechanical drawings of the flow chamber. Further, we want to express our gratitude to Max Beckers and Florian Drechsler for insightful comments and discussions regarding NPS and the underlying sampling engine.
Materials
| Flowchamber preparation | |||
| Customized metall sample holder | self-built | n/a | |
| quartz-glass slides, 76 x 26 mm | Technical Glass Products | 26007 | |
| coverslips, 60 x 24 mm | Marienfeld | 101242 | |
| detergent, Hellmanex II | Hellma | 320.001 | |
| ultra-pure water from Synergy UV | Millipore | 2512600 | |
| Zepto plasma cleaner | Diener | n/a | |
| (3-aminopropyl)-triethoxysilane, p.a. | Sigma-Aldrich | A3648 | |
| methoxy PEG-succinimidyl valerate, 5 kDa | Laysan Bio Inc. | MPEG-SVA-5000-1g | |
| biotinylated PEG-succinimidyl valerate, 5 kDa | Laysan Bio Inc. | BIOTIN-PEG-SVA-5000 | |
| Sodium biocarbonate | Sigma-Aldrich | S5761 Sigma | |
| Sodium carbonate | Sigma-Aldrich | S2127 Sigma-Aldrich | |
| sealing film (Nescofilm) | Fisher Scientific | 12981805 | |
| Tygon Flexible Silicone Tubing, 0.8 mm ID, 2.4 mm OD | Saint-Gobain Performance Plastics | 720958 | |
| Fine-Bore Polyethylene Tubing, 0.58 mm ID, 0.96 mm OD (Smiths Medical) | Fisher Scientific | 12665497 | |
| Neutravidin | Life Technologies | A2666 | |
| Name | Company | Catalog Number | Comments |
| Total internal reflection fluorescence microscope | |||
| Nd:YAG Laser, 532 nm | Newport Spectra-Physics | EXLSR-532-100-CDRH | |
| diode-pumped solid-state laser, 491 nm, Calypso | Cobolt | 904010050 | |
| diode laser 643 nm, iBeam smart | Toptica | iBEAM-SMART-640-S | |
| dichroic mirror, 532 RDC | Chroma | F33-540 | |
| dichroic mirror, 476 RDC | Chroma | F33-476z | |
| acousto-optic tunable filter | AA Opto-Electronic | AOTFnC-VIS | |
| plano-convex cylindrical lens, f = 75 mm | Thorlabs | LJ1703L1-A | |
| plano-concave cylindrical, f = -300 mm | Thorlabs | ||
| prism, PS 991 | Thorlabs | PS991 | |
| focussing lens, f = 75 mm | Thorlabs | LA1608-B | |
| syringe pump, PHD 2000 | Harvard Apparatus | 70-2002 | |
| 2 stepper motors, Z812B | Thorlabs | Z812B | |
| piezoelectric actuator, PE4 | Thorlabs | PE4 | |
| IR diode laser | Edmund Optics | CPS808 | part of the autofocus system |
| dichroic mirror, 775 DCXR | Chroma | 775 DCXR | |
| position-sensing detector (PSD), PDP90A | Thorlabs | PDP90A | part of the autofocus system |
| water-immersion objective, Plan Apo 60X WI, NA 1.2 | Nikon | MRD07601 | |
| dichroic mirror, 645 DCXR | Chroma | 645 DCXR | part of the emission pathway |
| emission filter, 3RD550-510 | Omega Optical | 3RD550-510 | green channel in the emission pathway |
| emission filter, 3RD660-760 | Omega Optical | 3RD660-760 | red channel in the emission pathway |
| EMCCD camera, iXon+ DU897EBV | Andor | AND-20-00032 | |
| EMCCD camera, iXon3 DU897D-BV | Andor | AND-20-000141 | |
| Name | Company | Catalog Number | Comments |
| Miscellaneous | |||
| Varian 50 | Cary | UV-VIS spectrometer | |
| Fluorolog2 | SPEX | fluorescence spectrometer | |
| Solis (V4.15) | Andor | control software for the EM-CCD camera | |
| Apt user utility (V1.022) | Thorlabs | control software for the piezo-motors | |
| Norland Optical Adhesive 68 | Thorlabs | adhesive | |
| PC-AFN-0.8 Nile red | Kisker Biotech | avidin-coated fluorescent multispec beads | |
| Matlab | Mathworks | technical computing language for custon written software | |
| Origin (V9.0) | Originlab | scientific graphing and data analysis software | |
| Hellma 105-202-15-40 | Hellma | 105-202-15-40 | absorption cuvette of 1 cm path length |
| Hellma 105-251-15-40 | Hellma | 105-251-15-40 | fluorescence cuvette with 3 mm path length |
Referências
- Cheng, Y. Single-Particle Cryo-EM at Crystallographic Resolution. Cell. 161, 450-457 (2015).
- Garman, E. F. Developments in X-ray Crystallographic Structure Determination of Biological Macromolecules. Science. 343 (6175), 1102-1108 (2014).
- Sali, A. Outcome of the First wwPDB Hybrid/Integrative Methods Task Force Workshop. Structure. 23, 1156-1167 (2015).
- Hopfner, K. P., Michaelis, J. Mechanisms of nucleic acid translocases: lessons from structural biology and single-molecule biophysics. Curr Opin Struct Biol. 17, 87-95 (2007).
- Ando, T., Uchihashi, T., Kodera, N. High-speed AFM and applications to biomolecular systems. Annu Rev Biophys. 42, 393-414 (2013).
- Neuman, K. K. C., Nagy, A. Single-molecule force spectroscopy: optical tweezers, magnetic tweezers and atomic force microscopy. Nat Methods. 5, 491-505 (2008).
- Yildiz, A. Myosin V walks hand-over-hand: single fluorophore imaging with 1.5-nm localization. Science. 300 (5628), 2061-2065 (2003).
- Joo, C., Balci, H., Ishitsuka, Y., Buranachai, C., Ha, T. Advances in Single-Molecule Fluorescence Methods for Molecular Biology. Annu Rev Biochem. 77 (1), 51-76 (2008).
- Hohlbein, J., Craggs, T. D., Cordes, T. Alternating-laser excitation: single-molecule FRET and beyond. Chem Soc Rev. 43 (4), 1156-1171 (2014).
- Stryer, L., Haugland, R. P. Energy transfer: a spectroscopic ruler. Proc Natl Acad Sci U S A. 58 (2), 719-726 (1967).
- Rasnik, I., Myong, S., Cheng, W., Lohman, T. M., Ha, T. DNA-binding Orientation and Domain Conformation of the E. coli Rep Helicase Monomer Bound to a Partial Duplex Junction: Single-molecule Studies of Fluorescently Labeled Enzymes. J Mol Biol. 336 (2), 395-408 (2004).
- Andrecka, J. Single-molecule tracking of mRNA exiting from RNA polymerase II. Proc Natl Acad Sci U S A. 105 (1), 135-140 (2008).
- Schröder, G. F., Grubmüller, H. FRETsg: Biomolecular structure model building from multiple FRET experiments. Comput Phys Commun. 158 (3), 150-157 (2004).
- Margittai, M. Single-molecule fluorescence resonance energy transfer reveals a dynamic equilibrium between closed and open conformations of syntaxin 1. Proc Natl Acad Sci U S A. 100 (26), 15516-15521 (2003).
- Kalinin, S. A toolkit and benchmark study for FRET-restrained high-precision structural modeling. Nat Methods. 9 (12), 1218-1227 (2012).
- Choi, J. N6-methyladenosine in mRNA disrupts tRNA selection and translation-elongation dynamics. Nat Struct Mol Biol. 23 (August 2015), 110-115 (2015).
- Svensson, B. FRET-based trilateration of probes bound within functional ryanodine receptors. Biophys J. 107 (9), 2037-2048 (2014).
- Stephenson, J. D., Kenyon, J. C., Symmons, M. F., Lever, A. M. L. Characterizing 3D RNA structure by single molecule FRET. Methods. (2016), 1-11 (2016).
- Lee, N. K. Accurate FRET measurements within single diffusing biomolecules using alternating-laser excitation. Biophys J. 88 (4), 2939-2953 (2005).
- McCann, J. J., Choi, U. B., Zheng, L., Weninger, K., Bowen, M. E. Optimizing methods to recover absolute FRET efficiency from immobilized single molecules. Biophys J. 99 (3), 961-970 (2010).
- Brunger, A. T., Strop, P., Vrljic, M., Chu, S., Weninger, K. R. Three-dimensional molecular modeling with single molecule FRET. J Struct Biol. 173, 497-505 (2011).
- Schuler, B. Single-molecule FRET of protein structure and dynamics – a primer. J nanoboitechnology. 11, 1-17 (2013).
- Choi, U. B. Single-molecule FRET-derived model of the synaptotagmin 1-SNARE fusion complex. Nat Struct Mol Biol. 17 (3), 318-324 (2010).
- Dale, R. E., Eisinger, J., Blumberg, W. E. The orientational freedom of molecular probes. The orientation factor in intramolecular energy transfer. Biophys J. 26 (2), 161-193 (1979).
- Kapanidis, A. N. Alternating-laser excitation of single molecules. Acc Chem Res. 38 (7), 523-533 (2005).
- Muschielok, A. A nano-positioning system for macromolecular structural analysis. Nat Methods. 5 (11), 965-971 (2008).
- Muschielok, A., Michaelis, J. Application of the nano-positioning system to the analysis of fluorescence resonance energy transfer networks. J Phys Chem B. 115 (41), 11927-11937 (2011).
- Andrecka, J. Nano positioning system reveals the course of upstream and nontemplate DNA within the RNA polymerase ii elongation complex. Nucleic Acids Res. 37 (17), 5803-5809 (2009).
- Treutlein, B. Dynamic Architecture of a Minimal RNA Polymerase II Open Promoter Complex. Mol Cell. 46 (2), 136-146 (2012).
- Nagy, J. Complete architecture of the archaeal RNA polymerase open complex from single-molecule. FRET and NPS. Nat Commun. 6, 6161 (2015).
- Grohmann, D., et al. The Initiation Factor TFE and the Elongation Factor Spt4/5 Compete for the RNAP Clamp during Transcription Initiation and Elongation. Mol Cell. 43 (2), 263-274 (2011).
- Beckers, M., Drechsler, F., Eilert, T., Nagy, J., Michaelis, J. Quantitative structural information from single-molecule FRET. Faraday Discuss. 184, 117-129 (2015).
- Bennink, M. L. Unfolding individual nucleosomes by stretching single chromatin fibers with optical tweezers. Nat Struct Biol. 8 (7), 606-610 (2001).
- Chandradoss, S. D. Surface passivation for single-molecule protein studies. J Vis Exp. (86), e50549 (2014).
- Würth, C., Grabolle, M., Pauli, J., Spieles, M., Resch-Genger, U. Relative and absolute determination of fluorescence quantum yields of transparent samples. Nat Protoc. 8 (8), 1535-1550 (2013).
- Lakowicz, J. R. . Principles of Fluorescence Spectroscopy. , (2006).
- Korkhin, Y. Evolution of complex RNA polymerases: The complete archaeal RNA polymerase structure. PLoS Biol. 7 (5), (2009).

