19.2:
Tipi di radioattività
12,513 Views
•
•
I tipi più comuni di radioattività sono il decadimento α, il β, il decadimento γ, l’emissione di neutroni e la cattura elettronica.
Il decadimento alfa (α) è l’emissione di α particella dal nucleo. Ad esempio, il polonio-210 subisce α decadimento:
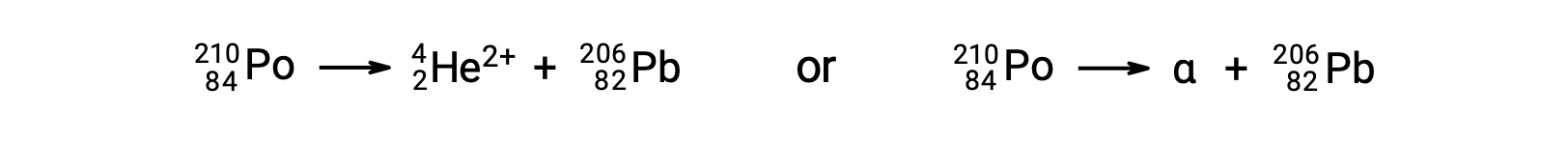
Il decadimento alfa avviene principalmente nei nucleipesanti (A > 200, Z > 83). La perdita di α particella dà un nuclide figlia con una massa di quattro unità più piccola e un numero atomico due unità più piccole di quelle del nuclide genitore.
Il decadimento beta (β) è l’emissione di un elettrone o positrone da un nucleo. Lo iodio-131 è un esempio di nuclide che subisce β− decadimento:
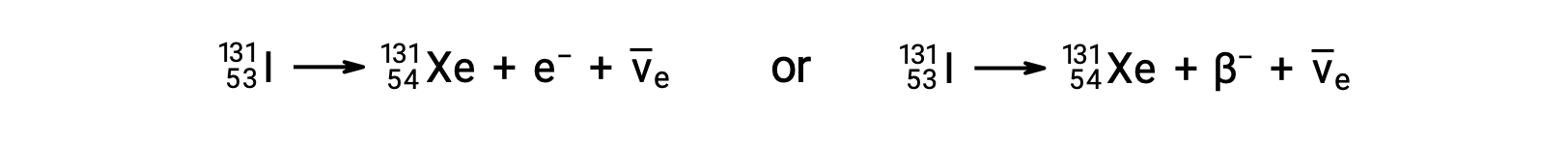
L’elettrone emesso proviene dal nucleo atomico e non è uno degli elettroni che circondano il nucleo. L’emissione di un elettrone non cambia il numero di massa del nuclide, ma aumenta il numero dei suoi protoni e diminuisce il numero dei suoi neutroni. Un antineutrino 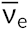 viene emesso anche a causa della conservazione dell’energia.
viene emesso anche a causa della conservazione dell’energia.
Ossigeno-15 è un esempio di nuclide che subisce emissione di positroni, o β+ decadimento:
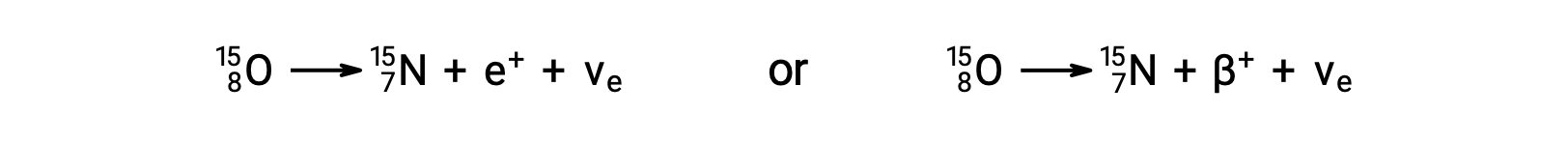
Il decadimento del positrone è la conversione di un protone in un neutrone con l’emissione di un positrone. Un neutrino (νe)viene emesso anche a causa della conservazione dell’energia.
L’emissione gamma (γ emissione) si osserva quando un nuclide si forma in uno stato eccitato e poi decade al suo stato suolo con l’emissione di un raggio γ, un quantico di radiazione elettromagnetica ad alta energia. La presenza di un nucleo in uno stato eccitato è spesso indicata da un asterisco (*). Il cobalto-60 emette γ radiazioni ed è utilizzato in molte applicazioni, incluso il trattamento del cancro:

Non vi è alcun cambiamento nel numero di massa o nel numero atomico durante l’emissione di γ raggi. Tuttavia, γ’emissione può accompagnare uno degli altri modi di decadimento che comporterebbe un cambiamento nel numero di massa o nel numero atomico.
L’emissione di neutroni è l’espulsione di un neutrone dal nucleo. Può accadere spontaneamente, come il decadimento del berillio-13 al berillio-12, o in risposta al bombardamento da parte di raggi gamma o particelle. Il numero atomico rimane invariato durante questo processo, mentre il numero di massa diminuisce di 1.
La cattura elettronica si verifica quando uno degli elettroni interni in un atomo viene catturato dal nucleo dell’atomo. Ad esempio, il potassio-40 subisce la cattura elettronica:
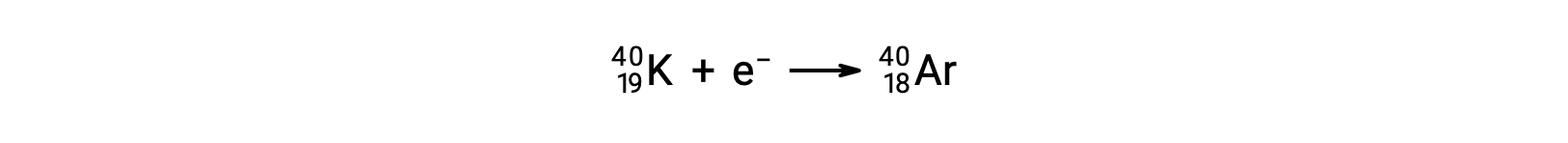
La cattura elettronica si verifica quando un elettrone a guscio interno si combina con un protone e viene convertito in un neutrone. La perdita di un elettrone a guscio interno lascia un posto vacante che sarà riempito da uno degli elettroni esterni. Quando l’elettrone esterno scende nel posto vacante, emetterà energia. Nella maggior parte dei casi, l’energia emessa sarà sotto forma di raggi X. La cattura elettronica ha lo stesso effetto sul nucleo dell’emissione di positroni: il numero atomico è diminuito di uno e il numero di massa non cambia.
Questo testo è adattato da Openstax, Chemistry 2e, Section 21.3: Radioactive Decay.
