3.3:
Modelli molecolari
34,272 Views
•
•
I modelli fisici che rappresentano architetture molecolari di composti chimici svolgono un ruolo essenziale nella comprensione della chimica. L’uso di modelli molecolari rende più facile visualizzare le strutture e le forme di atomi e molecole.
Modello scheletrico
Rappresentazioni bidimensionali più semplici di composti chimici vengono eseguite utilizzando modelli scheletrici. L’illustrazione mostra solo la struttura molecolare o i legami senza mostrare esplicitamente gli atomi. In questa rappresentazione, molti degli atomi di carbonio e degli atomi di idrogeno non sono esplicitamente mostrati. Tuttavia, le posizioni degli atomi sono implicite nelle giunzioni o nelle estremità dei legami. Questo modello aiuta a rappresentare strutture chimiche più grandi e complesse.
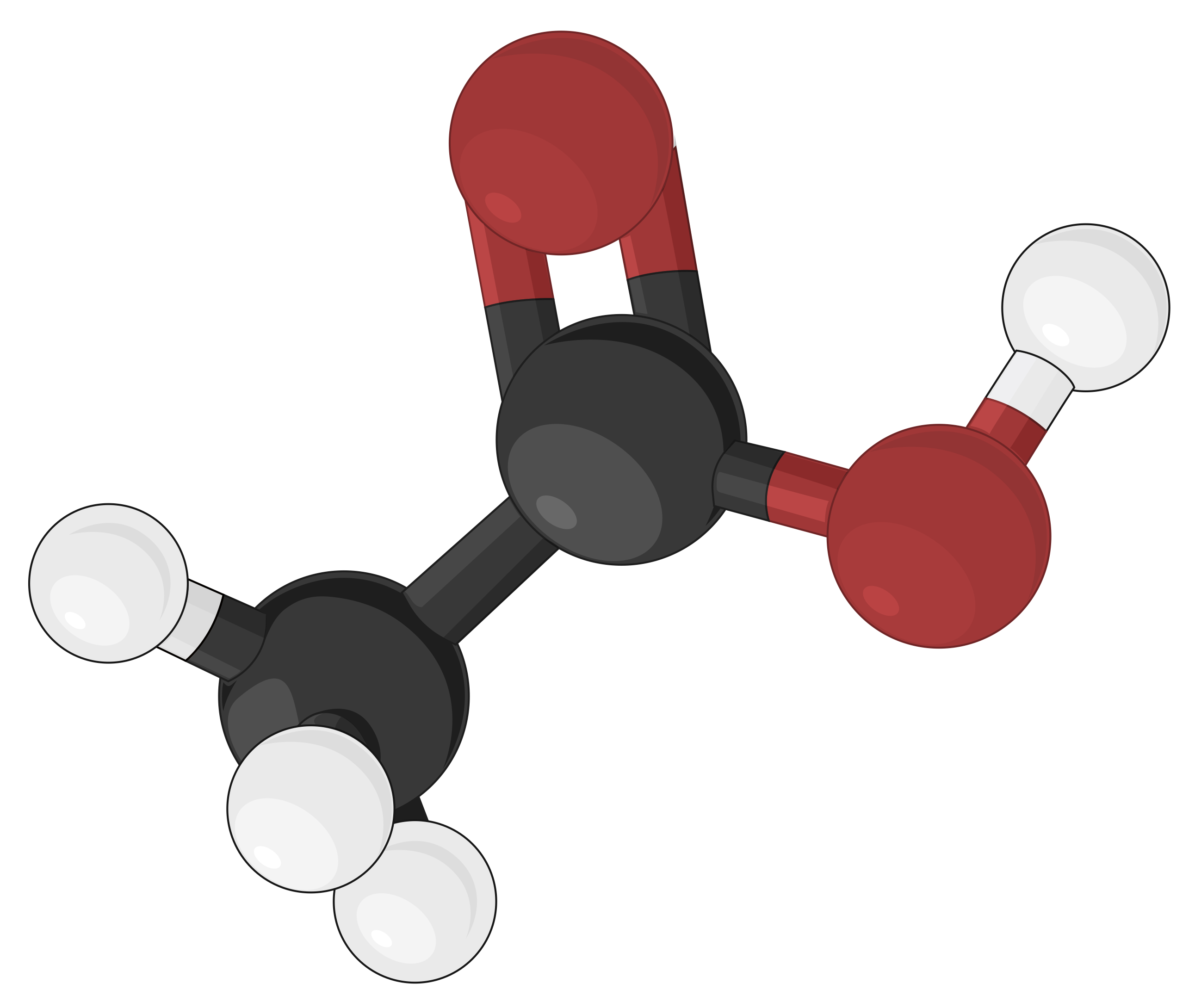
Modello a sfera e bastone
I modelli a sfera e bastone sono modelli tridimensionali, in cui gli atomi sono raffigurati come sfere o sfere codificate a colori, specifiche per diversi elementi. I legami chimici che collegano gli atomi sono rappresentati da aste e sono più facili da visualizzare. In questo modo, le dimensioni delle sfere sono rese relativamente più piccole, compromettendo così la correlazione proporzionale con la dimensione atomica effettiva. Tuttavia, il modello a sfera definisce gli angoli tra gli atomi, descrivendo chiaramente la geometria molecolare di strutture da semplici a più complesse rispetto ad altri modelli molecolari.
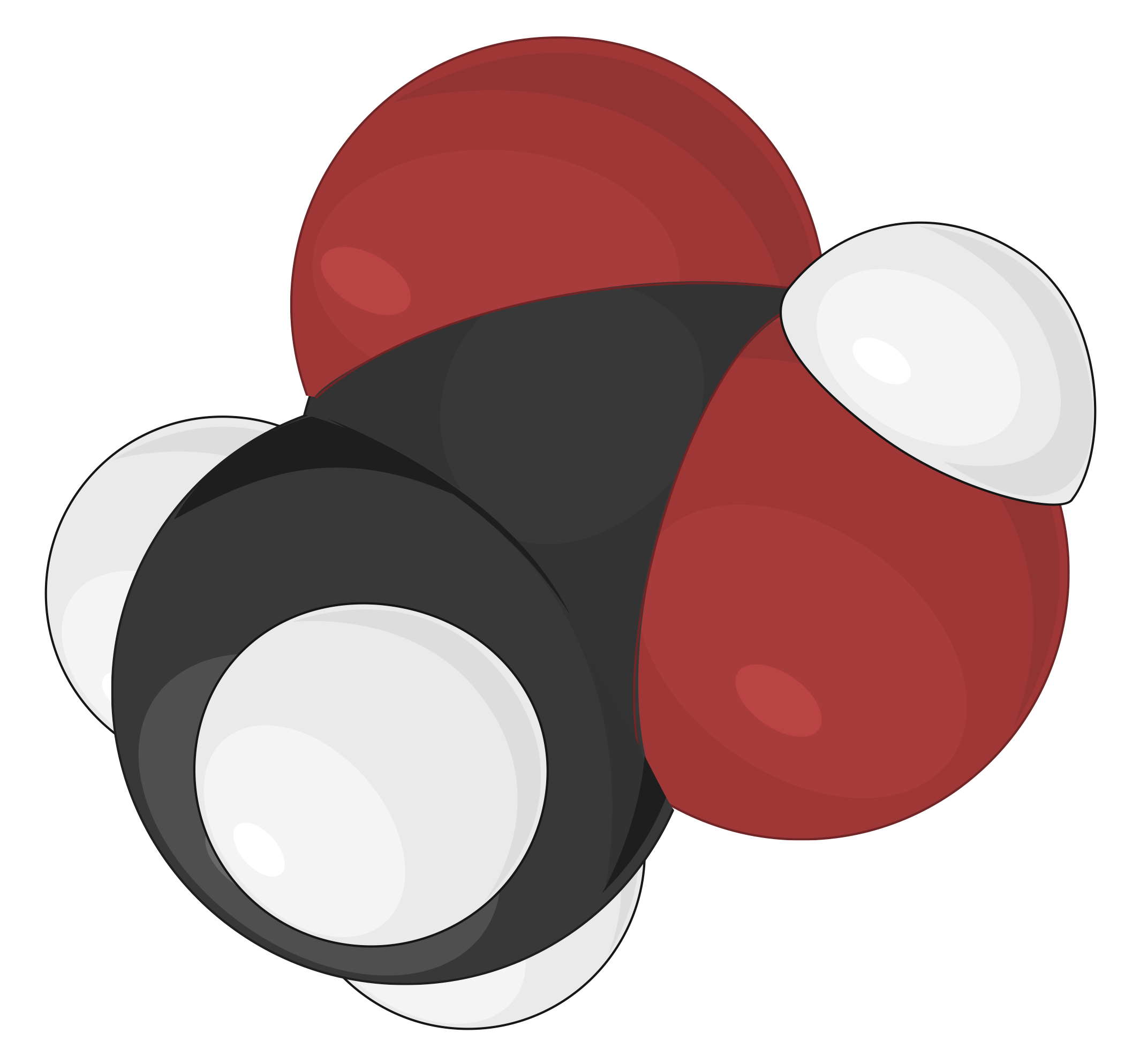
Modello di riempimento dello spazio
I modelli di riempimento dello spazio sono più realistici, dove gli atomi sono scalati in dimensioni per riempire lo spazio tra loro. Le dimensioni e la posizione di un atomo in questo modello sono determinate dalle sue proprietà di legame e dal raggio di van der Waals, o distanza di contatto. Il raggio di van der Waals descrive quanto due atomi possano avvicinarsi l’uno all’altro quando un legame covalente non li collega. Le sfere di questo modello illustrano lo spazio relativo occupato da ogni atomo all’interno di un composto, mentre gli angoli tra gli atomi non sono chiaramente visibili
Progettata per la prima volta dai chimici Robert Corey e Linus Pauling, e successivamente migliorata da Walter Koltun, la convenzione di colorazione CPK designa colori specifici per gli atomi di ogni elemento. Ad esempio, secondo la convenzione CPK, tutti gli atomi di idrogeno sono colorati di bianco, gli atomi di carbonio sono neri, gli atomi di azoto sono blu, gli atomi di ossigeno sono rossi, gli atomi di zolfo sono gialli profondi e gli atomi di fosforo sono viola. I metalli alcalini della terra sono rappresentati dal verde scuro e i metalli alcalini sono indicati dal viola.
Ad esempio, diversi modelli molecolari di acido acetico (CH3COOH) possono essere rappresentati nei seguenti modi:
 |
 |
|
| Modello scheletrico | Modello a sfera e bastone | Modello di riempimento dello spazio |
Questo testo è apted da: Openstax, Chimica 2e, Sezione 2.4: Formule chimiche.
