16.2:
완충용액
154,616 Views
•
•
약한 컨쥬게이트 산염 염기 쌍의 상당한 양을 포함하는 용액을 버퍼 용액 또는 버퍼라고 합니다. 완충액은 소량의 강한 산또는 강한 염기가 첨가될 때 pH의 변화에 저항합니다. 아세트산과 아세테이트 나트륨의 용액은 약한 산과 그 염으로 구성된 완충제의 예입니다: CH3COOH(aq)+ CH3COONa(aq). 약기와 염분으로 구성된 완충제의 예는 암모니아 및 염화암모늄의 용액입니다: NH3 (aq)+ NH4Cl(aq).
버퍼 작동 방식
완충액의 기능을 설명하기 위해 아세트산과 아세테이트 나트륨의 대략 동일한 양의 혼합물을 고려하십시오. 용액에 약한 컨쥬게이트 산염 염기 쌍의 존재는 적당한 양의 강한 산 또는 염기를 중화시키는 기능을 부여합니다. 예를 들어, 이 솔루션에 강한 기지를 추가하면 하이드로늄 이온을 중화하고 아세트산 이온화 평형을 오른쪽으로 이동하여 감소된 H3O+ 농도를 부분적으로 복원합니다.
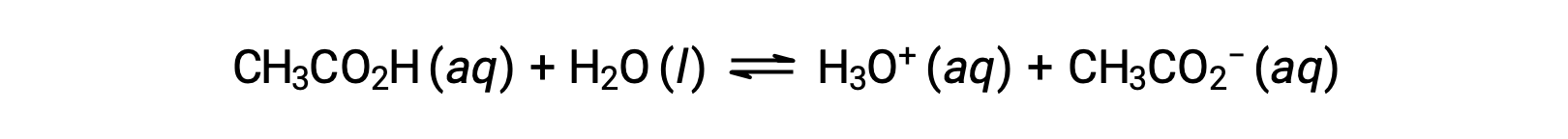
마찬가지로, 이 완충 액액에 강한 산을 추가하면 아세테이트 이온을 중화시키고 위의 이온화 평형을 오른쪽으로 이동하고 [H3O+]원래 값에 가깝게 되돌아갑니다. 도 1은 강한 산및 염기를 추가할 때 완충액의 변화에 대한 그래픽 그림을 제공합니다. 용액의 버퍼링 동작은 본질적으로 완충제의 컨쥬게이트 쌍을 구성하는 약한 산 및 염기로 변환되는 강한 산 및 염기가 첨가된 결과입니다. 약한 산및 염기는 강한 산및 염기의 완전한 이온화에 비해 약간의 이온화를 겪습니다. 따라서 솔루션 pH는 버퍼링되지 않은 솔루션보다 훨씬 덜 크게 변경됩니다.

그림 1. 아세트산과 아세테이트 염을 혼합하여 완충 작용을 합니다.
